Ampliando a visão sobre as funções das mitocôndrias
Acesso rápido
Mitocôndrias e relógio biológico
Disfunção mitocondrial e câncer
Nutrientes que impulsionam as mitocôndrias
L-carnitina na resistência à insulina e na beta-oxidação de gorduras
L-carnitina e sensação de saciedade
L-carnitina e idosos
Dano muscular causado por exercícios
Fadiga induzida por exercício
Estilo de vida e mitocôndrias
Exercício físico
Exposição ao frio
A função mitocondrial vai muito além da vital produção energética. A autodigestão celular por autofagia, por exemplo, que está emergindo como uma via biológica central que funciona para promover a saúde e a longevidade, tem início nas mitocôndrias. Essas e outras descobertas, apontadas por estudos, ampliam o papel das mitocôndrias, ligando-as ao ritmo do processo de envelhecimento.
Ao mesmo tempo, mais e mais nutrientes vêm sendo apontados como impulsionadores do bom funcionamento dessas organelas, ampliando não apenas a produção de ATP, mas também a proteção contra doenças não-transmissíveis.
Mas como isso ocorre? Além da respiração celular, quais são os outros processos em que a mitocôndria está envolvida? Quais nutrientes demonstram potencial para impulsionar o funcionamento dessas organelas? Quais são os efeitos dessa melhora? Confira no texto.
Por que a mitocôndria
é tão importante?
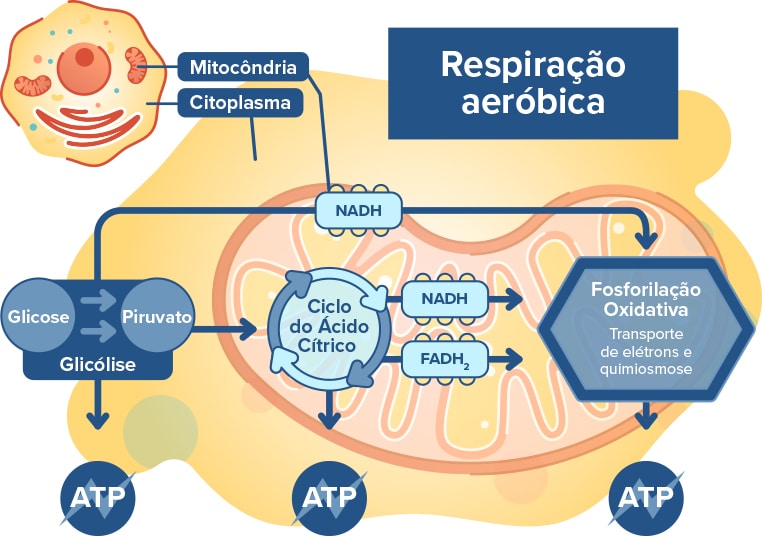
Se as mitocôndrias estivessem unicamente envolvidas na produção de ATP, elas já seriam uma das principais protagonistas da saúde humana, merecendo bastante atenção para a manutenção do seu perfeito funcionamento. No entanto, a mitocôndria controla também importantes funções que fazem o reparo e a limpeza de células e mitocôndrias não saudáveis, bem como de proteínas dentro das células, suprimindo o desenvolvimento de desequilíbrios e doenças crônicas:

Além disso, essas organelas estão intimamente envolvidas nas sínteses do heme, dos aminoácidos, dos lipídios e dos hormônios esteroides, no controle da concentração de íons de cálcio (Ca2+) dentro da célula, no ótimo funcionamento do exigente sistema imunológico e nervoso e no destino das células.
Mitocôndrias e relógio biológico
A disfunção mitocondrial, caracterizada por uma perda de eficiência na cadeia de transporte de elétrons e reduções na síntese de ATP, é uma característica do envelhecimento e, essencialmente, de todas as doenças crônicas. Confira como isso ocorre.
Uma pequena produção de espécies reativas de oxigênio é comum entre as mitocôndrias. Esse subproduto da organela é normalmente neutralizado pelo sistema de defesa antioxidante. Porém, mutações ocorridas no genoma mitocondrial alteram seu metabolismo, reduzindo a produção de ATP e predispondo a célula ao envelhecimento e a diversas doenças associadas.
Além disso, quadros de estresse oxidativo causados por outros fatores, como o consumo excessivo de álcool e a ingestão de alimentos contaminados por pesticidas, por exemplo, também afetam o funcionamento das mitocôndrias. Com a redução da integridade funcional das mitocôndrias há um aumento da produção de radicais livres e espécies reativas, o que pode induzir quadros de estresse oxidativo.
Essa cascata de fatos caracteriza as mitocôndrias como protagonistas do processo de envelhecimento, que o Dr. Denham Harman (1916 – 2014), gerontologista e cientista, conhecido como o pai da teoria do envelhecimento por ação dos radicais livres, em 1954, chamou de “relógio biológico”.
Disfunção mitocondrial e câncer
Uma compreensão sobre os vários tipos de câncer os definem como uma doença metabólica mitocondrial. Como todas as células cancerosas têm em comum a remodelação mitocondrial, essa hipótese defende a restauração da função mitocondrial como uma estratégia contra os cânceres.
Ao produzir um excesso de espécies reativas, a mitocôndria disfuncional gera um quadro oxidativo que causa mutações no DNA nucleico da célula e no DNA mitocondrial. O DNA nucleico é protegido contra os radicais livres pelas histonas, ao contrário do DNA mitocondrial, o que o torna mais suscetível ao dano oxidativo.
Assim, os mecanismos genético-moleculares implicados na gênese e na progressão do câncer estão sendo repensados com essa teoria. A hipótese atual é que não são as mutações genéticas a raiz causal do câncer, ou não somente, mas que o excesso de danos mitocondriais acontece primeiramente.
Nutrientes que impulsionam as mitocôndrias
Diversos micronutrientes são apontados como impulsionadores do funcionamento mitocondrial. Neste texto, no entanto, vamos nos ater a dois deles, com ampla literatura de apoio: L-carnitina e Coenzima Q10.

A carnitina (L-3-hidroxitrimetilaminobutanoato) é um composto de ocorrência natural encontrado em todas as células do corpo, mas particularmente abundante no músculo esquelético e no miocárdio.
A carnitina, uma amina quaternária(3-hidroxi-4-N-trimetilamino-butirato), é sintetizada no organismo (fígado, rins e cérebro) a partir de dois aminoácidos essenciais: lisina e metionina, exigindo para sua síntese a presença de ferro, ácido ascórbico, niacina e vitamina B6.
Pode também ser ingerida através da alimentação. As fontes primárias de carnitina na dieta são carne vermelha e laticínios. Ao mesmo tempo, suplementos têm se mostrado fontes eficientes.
L-carnitina na resistência à insulina
e na beta-oxidação de gorduras
A suplementação de L-carnitina pode melhorar os parâmetros do metabolismo da insulina, modulando a expressão de enzimas glicolíticas e gluconeogênicas. Assim, melhora a oxidação da glicose mitocondrial. Também age como uma molécula de transporte de ácidos graxos de cadeia longa através da membrana mitocondrial interna, atuando como um cofator obrigatório para a ß-oxidação de ácidos graxos. Por causa desses dois efeitos da L-carnitina no metabolismo da glicose e dos lipídeos, ela pode auxiliar na perda de peso por aumentar o gasto energético.
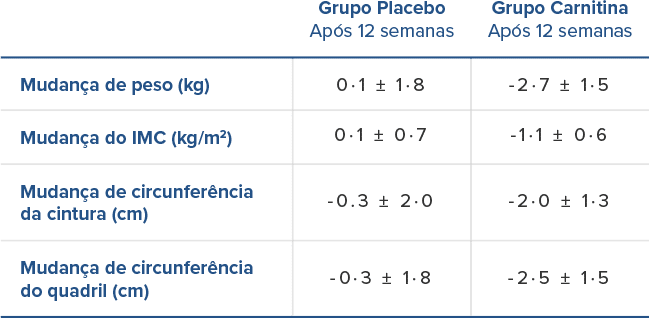
Segundo estudo publicado em Clinical Endocrinology, a suplementação com L-carnitina gerou efeitos benéficos sobre o peso, IMC, circunferência da cintura, circunferência do quadril e controle glicêmico de mulheres diagnosticadas com Síndrome do Ovário Policístico.
L-carnitina e sensação de saciedade
Ao facilitar a oxidação de ácidos graxos, a L-carnitina contribui para a produção de energia e impulsiona a principal adaptação metabólica à inanição, que é a mobilização lipídica.
Estudo clínico em pacientes com síndrome metabólica mostrou que a suplementação com L-carnitina levou a uma redução gradativa na percepção da fome.

A L-carnitina reduziu ainda a fadiga física e mental e os escores de gravidade da fadiga durante a inanição. Por outro lado, o grupo de controle registrou aumento significativo na pontuação de fome, em comparação com a linha de base.
L-carnitina e idosos
Entre todas as substâncias que têm a concentração diminuída com a idade, a L-carnitina é fundamentalmente importante, dada sua função na produção de energia. Uma das consequências mais importantes da deficiência de carnitina manifesta-se, portanto, na alteração das vias metabólicas que conduzem à produção de energia.
No tecido cerebral, a L-carnitina medeia a translocação da porção acetil da mitocôndria para o citosol e, assim, contribui para a síntese de acetilcolina e de acetilcarnitina. Os efeitos neurobiológicos da acetilcarnitina incluem a modulação da energia cerebral e o metabolismo dos fosfolipídios, macromoléculas celulares (tais como fatores neurotróficos e neurohormônios), morfologia sináptica e transmissão sináptica de vários neurotransmissores.
Estudo realizado com 70 indivíduos com mais de 100 anos mostrou, após seis meses de suplementação, que a L-carnitina atua na redução da massa gorda total e no aumento da massa muscular total, o que facilita um aumento da capacidade de atividade física e cognitiva, reduzindo a fadiga e melhorando as funções cognitivas.

Coenzima Q10 é encontrada em grande concentração nas mitocôndrias, onde oferece proteção antioxidante nas membranas. Além disso, é componente-chave na cadeia de transporte de elétrons, necessária para a síntese de ATP.
Estudos mostram que aumentar os níveis dessa coenzima através da suplementação melhora o transporte de elétrons mitocondriais, independentemente das células estarem deficientes dela ou não.
Assim como a L-carnitina, a Coenzima Q10 tem sua produção diminuída no organismo como parte do processo de envelhecimento.
Dano muscular causado por exercícios
Como a CoQ10 está localizada nas membranas próximas às cadeias lipídicas insaturadas, ela atua como um necrófago primário de espécies reativas de oxigênio e evita a peroxidação lipídica. Com isso, atua como um mediador do processo de fagocitose do tecido muscular lesionado em atividades físicas, ajudando a evitar que o excesso de espécies reativas de oxigênio danifique tecidos saudáveis.
Estudo com atletas da arte marcial Kendo, submetidos a 5 dias de treinamento intenso e suplementados com Coenzima Q10, mostrou redução dos níveis séricos de creatina quinase e mioglobina, marcadores de danos ao músculo esquelético.


Fadiga induzida por exercício
Composto indispensável na cadeia respiratória da membrana mitocondrial, a Coenzima Q10 também atua como um antioxidante essencial, auxiliando na regeneração de outros antioxidantes. Por outro lado, a redução nos substratos de energia, a proliferação de espécies reativas de oxigênio e a oxidação de proteínas são características da fadiga induzida por exercício.
Estudo publicado em Nutrition examinou os efeitos da suplementação com Coenzima Q10 na sensação de fadiga induzida por exercício. Ao todo, 17 voluntários saudáveis foram submetidos a atividades físicas exaustivas e tiveram seu nível de fadiga medidos antes da atividade, logo após sua conclusão e após o período de recuperação.

Estilo de vida e mitocôndrias
Como vimos ao longo do texto, quanto mais mitocôndrias saudáveis, mais energia e saúde. Além dos nutrientes específicos, é possível estimular a biogênese mitocondrial através de práticas como o exercício aeróbico intenso, restrição calórica, exposição ao frio e a adoção de uma dieta cetogênica. Rica em gorduras saudáveis, moderada em proteínas e pobre em carboidratos, essa dieta aumenta os corpos cetônicos circulantes enquanto reduz os níveis de açúcar no sangue.
Os corpos cetônicos (acetoacetato, beta-hidroxibutirato e acetona) são moléculas de energia solúveis em água, produzidas pelas mitocôndrias no fígado a partir de gorduras dietéticas disponíveis ou armazenadas. Essas moléculas ignoram a glicólise, entram nas mitocôndrias diretamente para a oxidação e são uma fonte de energia alternativa viável para as células com função mitocondrial normal.
Além disso, os corpos cetônicos reduzem a produção de espécies reativas de oxigênio, enquanto aumentam a atividade da glutationa peroxidase, um dos sistemas endógenos de defesa antioxidante. Também reduzem as citocinas pró-inflamatórias e aumentam as citocinas anti-inflamatórias.
Exercício físico
O exercício físico eleva a temperatura corporal, gerando um estresse oxidativo momentâneo, e, como resposta, o aumento da função e do conteúdo mitocondrial nas células. Os estudos mostram que, de forma cíclica e adaptativa, a maior necessidade de energia acarreta na maior necessidade de mitocôndrias nas células musculares, o que estimula sua produção.
Exposição ao frio
Expor o corpo a baixas temperaturas o obriga a produzir mais calor para sobreviver. Assim, essa ação física gera um estímulo à produção mitocondrial principalmente no tecido gorduroso, aumentando a produção de gordura marrom – um tecido termogênico cuja principal função é a produção de calor quando ativado pela exposição ao frio.


EXCELENTE CONTEÚDO
Olá Dra Angela, agradecemos imensamente seu feedback ♥ Um grande abraço, Essentia Group