Hormônios andrógenos intramusculares
Acesso rápido
Resultados clínicos
Apresentações disponíveis
Indicações terapêuticas
Atuação no organismo
Testosterona base
Testosterona propionato
Testosterona cipionato
Testosterona undecanoato
Associação de hormônios
Principais efeitos da deficiência de hormônios andrógenos
Vias de administração
Aspectos importantes sobre a prescrição de hormônios andrógenos injetáveis
Referências
Introdução
O sistema endócrino desempenha um papel importante na regulação de diversas funções corporais, como o metabolismo, o equilíbrio energético, a reprodução, o comportamento e a adaptação às mudanças em ambientes internos e externos. Entre essas funções, o músculo esquelético é o órgão-alvo pelo qual o sistema endócrino tem o controle das diferentes atribuições do corpo. A massa muscular esquelética, por sua vez, é regulada principalmente pela prática de exercícios, pela nutrição e pela ação dos hormônios.
Entre os hormônios envolvidos nesse processo, a testosterona ocupa posição de destaque devido à sua atuação em múltiplos órgãos e funções do corpo. A testosterona é o principal hormônio andrógeno, sintetizado no testículo, ovário e córtex adrenal. No homem, desempenha papel essencial no desenvolvimento e na manutenção das características masculinas, incluindo massa muscular, massa óssea, libido, potência sexual e espermatogênese. Nas mulheres, a testosterona atua no desenvolvimento durante a fase puberal, na função sexual, na densidade óssea, na massa muscular, na eritropoiese, na energia, na função cognitiva e no humor.
Resultados clínicos
Com o objetivo de prolongar sua ação no organismo, foram desenvolvidos ésteres derivados da testosterona, os quais aumentam o tempo de atividade da molécula no metabolismo humano. Dessa forma, pode-se utilizar a testosterona base, estruturalmente semelhante à produzida naturalmente pelo organismo, ou optar por utilizar as testosteronas propionato, cipionato ou undecanoato, que proporcionam maior tempo de meia-vida e, consequentemente, demandam menor recorrência de aplicações.
Além da testosterona e seus ésteres, há também a nandrolona decanoato, um esteroide anabolizante que consiste em uma molécula similar à testosterona, perdendo apenas um grupo metil em sua estrutura química.
Apresentações disponíveis
- Testosterona base 25mg/1mL
- Testosterona base 50mg/1mL
- Testosterona base 100mg/2mL
- Testosterona cipionato 100mg/1mL
- Testosterona propionato 25mg/1mL
- Testosterona propionato 50mg/1mL
- Testosterona propionato 100mg/1mL
- Testosterona undecanoato 300mg/1mL
- Nandrolona decanoato 25mg/2mL
- Nandrolona decanoato 50mg/2mL
- Testosterona propionato 50mg + testosterona cipionato 100mg + testosterona undecanoato 100mg/1mL
Indicações terapêuticas
A reposição de hormônios andrógenos, quando conduzida de maneira adequada e cautelosa para corrigir a deficiência hormonal, pode auxiliar no aumento e estabilização da densidade óssea. Além disso, estudos relatam uma melhora na composição corporal, com consequente aumento da força muscular e redução do tecido adiposo. Também podem ser observados efeitos sobre a melhora do humor e do comportamento, bem como ações relacionadas à restauração e manutenção de características sexuais secundárias, incluindo a libido e a função erétil.
Atuação no organismo
O hipotálamo libera, a cada 60-90 minutos, o hormônio liberador de gonadotrofina (GnRH), que estimula a hipófise a produzir e secretar o hormônio folículo-estimulante (FSH) e o hormônio luteinizante (LH). O LH atua nas células de Leydig, responsáveis pela produção de testosterona, que se liga aos receptores androgênicos por meio da conversão de dois metabólitos ativos — di-hidrotestosterona e estradiol — pela ação das enzimas 5-α-redutase e aromatase, respectivamente.
Os testículos produzem em torno de 3 a 10mg de testosterona ao dia. Por se tratar de um hormônio esteroide derivado de lipoproteínas de baixa densidade (LDL), seu transporte pelo sangue depende de proteínas carreadoras, onde 58% da testosterona total está ligada à albumina, 40% à globulina ligadora de hormônios sexuais (SHBG) e apenas 2% está na sua forma livre. Considerando isso, somente essa fração livre da testosterona é disponibilizada para gerar a resposta biológica direta nos tecidos.
A aplicação intramuscular de testosterona tem sido amplamente utilizada para terapia de reposição. A esterificação da molécula no carbono da posição 17 prolonga a sua ação no organismo e promove uma maior solubilidade em meio oleoso, permitindo liberação gradativa do hormônio com aplicação via intramuscular. Quanto maior o número de carbonos da molécula, mais lentamente ela é liberada no depósito intramuscular, resultando em diferentes intervalos de aplicação.
A figura abaixo apresenta a molécula de testosterona base (A) e suas possíveis derivações para aumentar o seu tempo de meia-vida no organismo: testosterona propionato (B), cipionato (C) e undecanoato (D).
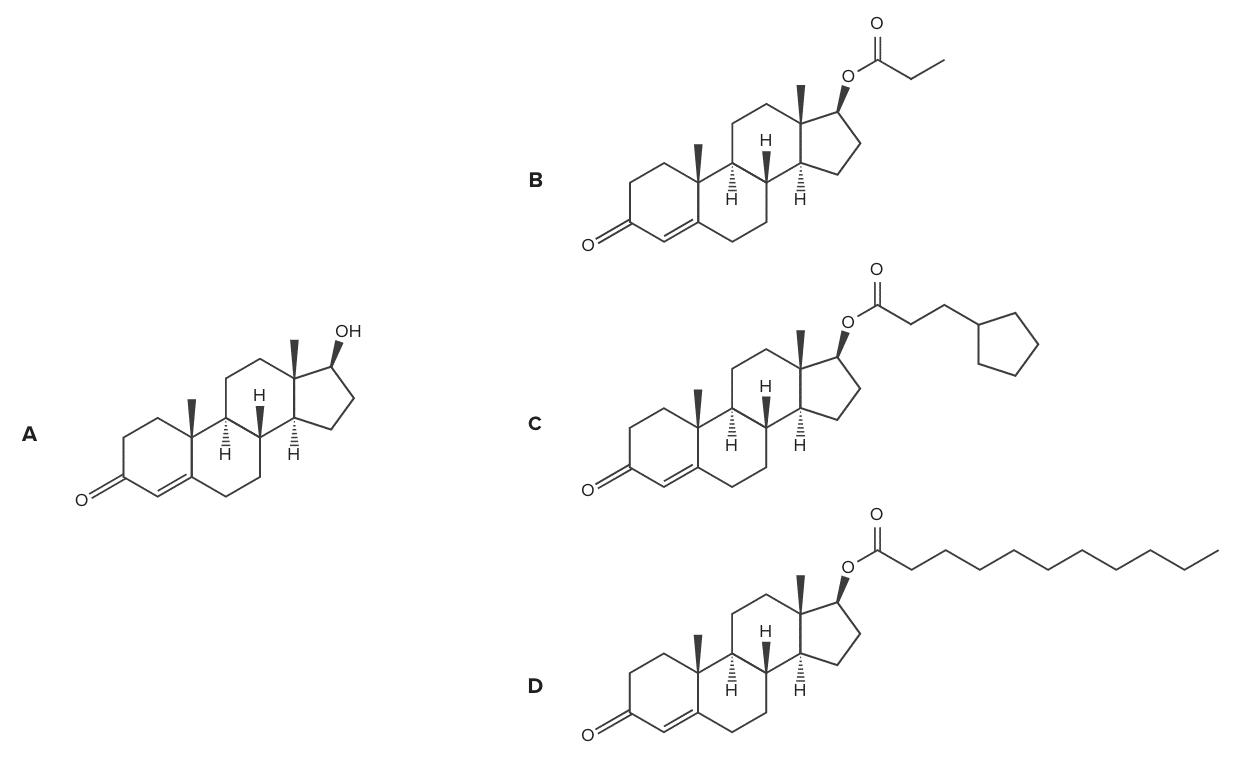
Figura 1: estruturas químicas da testosterona base e seus ésteres.
Testosterona base
A testosterona base (A) apresenta uma estrutura química semelhante à produzida de maneira endógena pelo corpo humano. É formulada em veículo oleoso, próprio para administração injetável, e apresenta característica de depósito no tecido muscular, onde o fármaco é gradativamente absorvido pelas fibras musculares.
Os estudos que avaliam a equivalência de doses entre as vias injetável e transdérmica ainda são escassos, assim como as literaturas que avaliam seu tempo de meia-vida — período em que a molécula atinge metade da concentração inicialmente administrada — e sua farmacocinética pela via intramuscular.
Diante disso, recomenda-se a aplicação semanal da testosterona base, realizando a dosagem dos níveis séricos antes da próxima administração para avaliar a resposta ao tratamento e realizar, se necessário, os ajustes adequados da dose.
Testosterona propionato
A testosterona propionato (B) contém uma cadeia carbônica maior que a molécula de testosterona base, o que resulta em um tempo de meia-vida mais prolongado, de aproximadamente 19 horas. Após uma única injeção de 50mg, a concentração máxima é atingida em cerca de 14 horas. Com base nesse perfil, os intervalos de aplicação recomendados variam entre 2 e 3 dias, com valores acima e abaixo da faixa considerada normal. Dessa forma, recomenda-se a aplicação semanal da testosterona propionato, realizando a dosagem dos níveis séricos antes da próxima administração, para avaliar a resposta ao tratamento e realizar, se necessário, os ajustes adequados na dose.
Testosterona cipionato
A meia-vida da testosterona cipionato (C) é de, aproximadamente, 8 dias quando administrada pela via intramuscular. É possível perceber que o aumento da cadeia carbônica resulta em um aumento gradativo do tempo de metabolização das moléculas. Com isso, é recomendada a sua aplicação em intervalos de 2 a 4 semanas.
Testosterona undecanoato
Para a aplicação de testosterona undecanoato ou undecilato (D) pela via intramuscular, recomenda-se a administração total de 1000mg em um intervalo de 10 a 14 semanas, a ser avaliado pelo prescritor. Ela apresenta um dos maiores tempos de meia-vida entre os ésteres de testosterona, possuindo uma cadeia molecular com 11 carbonos a mais que a testosterona base (A).
Associação de hormônios
A combinação dos ésteres testosterona propionato (B), testosterona cipionato (C) e testosterona undecanoato (D) em uma única formulação proporciona uma liberação gradual e sustentada dos hormônios, otimizando o perfil farmacocinético e reduzindo a frequência de aplicações necessárias para manter os níveis séricos dentro da faixa terapêutica.
A associação entre esses ésteres combina os benefícios de diferentes tempos de meia-vida, permitindo um início de ação mais rápido, devido a isoforma do propionato, e uma liberação prolongada, devido aos ésteres cipionato e undecanoato. Essa abordagem favorece tanto a eficácia terapêutica quanto a adesão ao tratamento, especialmente em pacientes que necessitam de reposição hormonal contínua, garantindo concentrações plasmáticas estáveis e minimizando as flutuações hormonais típicas de regimes com ésteres isolados.
Com base no tempo de liberação dos ativos individualmente, os intervalos de aplicação recomendados para a associação de testosterona variam de 3 a 4 semanas, sendo avaliados pelo prescritor mediante exames laboratoriais e acompanhamento dos níveis séricos.
As formulações que contêm testosterona undecanoato atingem o estado estacionário apenas após a terceira ou quinta aplicação. Por esse motivo, recomenda-se a dosagem dos níveis séricos no início da terceira semana de tratamento, com o objetivo de avaliar a resposta individual e, caso necessário, realizar ajustes de dose para melhor adequação clínica.
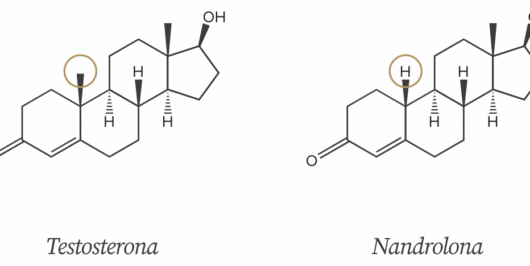
Figura 2: diferenças estruturais entre testosterona base e nandrolona base
A diferença entre a testosterona base e a nandrolona base é apenas a perda de um grupo metil durante a síntese de nandrolona. Enquanto o metabólito da testosterona, a di-hidrotestosterona, possui alta afinidade pela enzima 5-α-redutase, o metabólito da nandrolona, o 5α-dihydro-19-nortestosterone, possui menor afinidade por essa enzima.
Em um estudo que quantificou as atividades miotróficas androgênicas em animais, comparando diferentes tipos de hormônios andrógenos, a nandrolona demonstrou maior atividade anabólica do que a própria testosterona. Os autores relacionaram esse resultado ao metabolismo diferente das moléculas, que geram ativações com ações distintas nos tecidos androgênicos.
Por esse motivo, a nandrolona tem sido utilizada em uma variedade de indicações clínicas, incluindo os tratamentos de hipogonodismo, distrofia muscular, recuperação de fraturas ósseas, doença obstrutiva pulmonar crônica, anemia, reversão da perda de tecido magro em mulheres com HIV e outras condições catabólicas crônicas.
A nandrolona base possui tempo de meia-vida aproximado de 4 horas. Já em sua forma esterificada, o Decanoato de Nandrolona (conforme ilustrado na imagem a seguir), apresenta o tempo de meia-vida em torno de 7 dias.
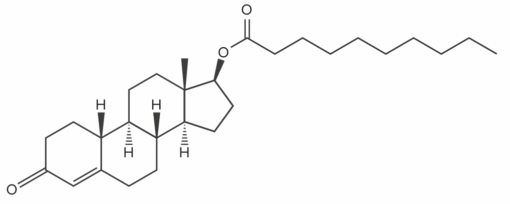
Figura 3: estrutura química da nandrolona decanoato
Principais efeitos da deficiência de hormônios andrógenos
O hipogonadismo é a condição clínica na qual baixos níveis de hormônios andrógenos séricos são encontrados em associação com sinais e sintomas característicos, como: baixa libido, disfunção erétil, sintomas sexuais, falta de energia, baixa sensação de vitalidade e bem-estar, aumento da fadiga, humor deprimido, cognição prejudicada, diminuição de massa e força muscular, densidade óssea diminuída e anemia.
Vias de administração
Os hormônios injetáveis devem ser aplicados exclusivamente por via intramuscular. Uma das formas farmacêuticas mais utilizadas na terapia de reposição para aplicações dos hormônios andrógenos é a solução oleosa, formando um depósito muscular.
A esterificação aumenta a lipossolubilidade dos hormônios, prolongando sua permanência no organismo. Após a aplicação, os ésteres são liberados no músculo e armazenados em depósitos de gordura, sendo posteriormente clivados para liberar os andrógenos em sua forma livre.
A administração intramuscular de hormônios em veículo oleoso deve ser feita pela via intramuscular profunda, com aplicação pela técnica em Z. Essa técnica é recomendada para todas as injeções intramusculares, uma vez que ajuda a reduzir a dor e o escape da medicação no local da entrada da agulha. A injeção deve ser feita a uma velocidade de 1mL a cada 10 segundos, permitindo que as fibras musculares se expandam adequadamente e contenham a solução oleosa.
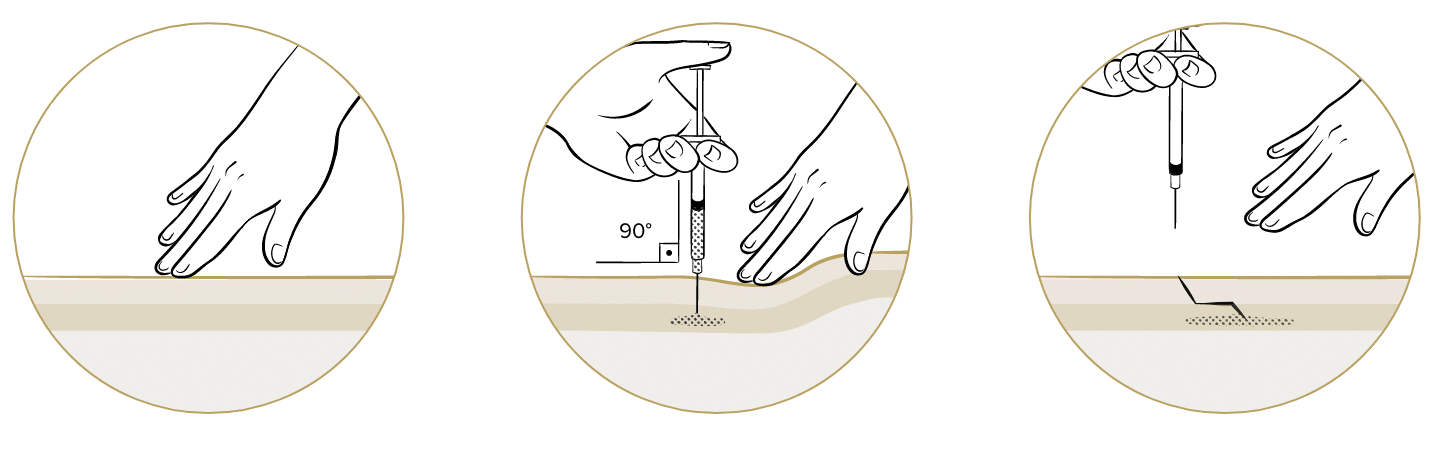
A seleção do local da injeção e o calibre da agulha também são importantes para a aplicação correta, sendo necessário avaliar os locais que apresentem massa muscular suficiente para receber a aplicação. Conforme o Conselho Regional de Enfermagem de São Paulo (2010), a região ventroglútea é considerada a opção mais segura e de primeira escolha, uma vez que evita a punção acidental de vasos sanguíneos e nervos. A região dorsoglútea também é uma boa opção de aplicação de injeção intramuscular de veículos oleosos.
Aspectos importantes sobre a prescrição de hormônios andrógenos injetáveis
Os hormônios injetáveis são manipulados após o envio adequado da prescrição médica e a confirmação de cada pedido individualmente. A receita de controle especial deve conter todas as informações de acordo com a legislação vigente.
As solicitações recebidas seguem um fluxograma de manipulação de hormônios:
- Pedidos confirmados até às 12h de segunda-feira: manipulação realizada de terça a sexta-feira da mesma semana.
- Pedidos confirmados à partir das 12h de segunda-feira: manipulação realizada na semana seguinte.
Após o preparo, as formulações são mantidas em quarentena por 15 dias. Após esse tempo, são aprovadas pelo controle de qualidade e liberadas. O prazo para recebimento dos pedidos manipulados é, em média, de 25 a 30 dias.
IMPORTANTE
Este material é de apoio técnico para prescritores e é proibida a sua divulgação para consumidores, nos termos do item 5.14 da RDC 67/2007.
Martín, A. I., Priego, T., López-Calderón, A. (2018). Hormones and Muscle Atrophy. Muscle Atrophy, 207–233. doi:10.1007/978-981-13-1435-3_9
Leichtnam, M.-L., Rolland, H., Wüthrich, P., & Guy, R. H. (2006). Testosterone Hormone Replacement Therapy: State-of-the-Art and Emerging Technologies. Pharmaceutical Research, 23(6), 1117–1132. doi:10.1007/s11095-006-0072-5
Stárka, L., Duskova, M. (2019). What Is a Hormone?. Institute of Endocrinology, Prague, Czech Republic, Physiol. Res. 69 (Suppl. 2): S183-S185. doi: 10.33549/physiolres.934509
Nieschlag E., Nieschlag S. ENDOCRINE HISTORY: The history of discovery, synthesis and development of testosterone for clinical use. Eur J Endocrinol. 2019 Jun 1;180(6):R201-R212. doi: 10.1530/EJE-19-0071. PMID: 30959485.
Fonseca G., Dos Santos M., Souza F., Negrão C., Alves M. Testosterone And Cardiovascular Disease: From Treatment to Abuse. Journal of the Society of Cardiology of the State of São Paulo.(2019). 29. 393-399. doi: 10.29381/0103-8559/20192904393-9.
Hellstrom, W. J. G. (2004). Testosterone Replacement Therapy. The Scientific World JOURNAL, 4, 142–149. doi:10.1100/tsw.2004.60
Rastrelli, G., Reisman, Y., Ferri, S., Prontera, O., Sforza, A., Maggi, M., & Corona, G. (2018). Testosterone Replacement Therapy. Sexual Medicine, 79–93. doi:10.1007/978-981-13-1226-7_8
Pastuszak, A. W., Gittelman, M., Tursi, J. P., Jaffe, J. S., Schofield, D., & Miner, M. M. (2021). Pharmacokinetics of testosterone therapies in relation to diurnal variation of serum testosterone levels as men age. Andrology. doi:10.1111/andr.13108
Rhoden, E. L., & Morgentaler, A. (2004). Risks of Testosterone-Replacement Therapy and Recommendations for Monitoring. New England Journal of Medicine, 350(5), 482–492. doi:10.1056/nejmra022251
BRASIL. Ministério da Saúde/SNVS. Portaria n°344 de 12 de maio de 1998 Aprova o Regulamento Técnico sobre substâncias e medicamentos sujeitos a controle especial. Diário Oficial da República Federativa do Brasil. Brasília, 31 de dezembro de 1998.
Resolução da Diretoria Colegiada – RDC n° 357, de 24 de março de 2020, Estende, temporariamente, as quantidades máximas de medicamentos sujeitos a controle especial permitidas em Notificações de Receita e Receitas de Controle Especial e permite, temporariamente, a entrega remota definida por programa público específico e a entrega em domicílio de medicamentos sujeitos a controle especial, em virtude da Emergência de Saúde Pública de Importância Internacional (ESPII) relacionada ao novo Coronavírus (SARS-CoV-2. Diário Oficial da União, Poder Executivo, Brasília, DF, BRASIL. RDC no 357, de 24 de março de 2020.
Pan, M. M.; Kovac, J. R. (2016). Beyond testosterone cypionate: evidence behind the use of nandrolone in male health and wellness. Translational Andrology and Urology, 5 (2), 213-219. DOI: 10.21037/tau.2016.03.03
Tatem A. J. et al. (2019). Nandrolone decanoate relieves joint pain in hypogonadal men: a novel prospective pilot study and review of the literature. Translational Andrology and Urology, 9 (2), 186-194. DOI: 10.21037/tau.2019.11.03.
Yuen, M. V. et al. (2020). Nandrolone decanoate: Summary Report. University of Maryland Baltimore. UMB Digital Archive.
Soma, L. R. et al. Pharmacokinetics of boldenone and stanozolol and the results of quantification of anabolic and androgenic steroids in race horses and nonrace horses. J. vet. Pharmacol. Therap. 30, 101–108, 2007
Poelmans, S. et al. Analytical possibilities for the detection of stanozolol and its metabolites. Analytica Chimica Acta 473 (2002) 39–47.
Moeller, B. C. et al. Pharmacokinetics of stanozolol in Thoroughbred horses following intramuscular administration. J. vet. Pharmacol. Therap. doi: 10.1111/j.1365-2885.2012.01393.x
Hackney, A. C., & Constantini, N. W. (Eds.). (2020). Endocrinology of Physical Activity and Sport. Contemporary Endocrinology. doi:10.1007/978-3-030-33376-8
Maravelias, C. et al. Adverse effects of anabolic steroids in athletes - A constant threat. Toxicology Letters 158 (2005) 167–175. doi:10.1016/j.toxlet.2005.06.005
Kuhn, C. M. Anabolic Steroids. Department of Pharmacology and Cancer Biology, Duke University Medical Center.
Bosi, A. Androgen use in bone marrow failures and myeloid neoplasms: Mechanisms of action and a systematic review of clinical data. Blood Reviews 62 (2023) 101132. DOI: https://doi.org/10.1016/j.blre.2023.101132
Roman, M. et al. Computational Assessment of Pharmacokinetics and Biological
Effects of Some Anabolic and Androgen Steroids. Pharm Res. DOI: https://doi.org/10.1007/s11095-018-2353-1
Chaudhary, K. et al. Long-Acting Injectables: Current Perspectives and Future Promise. Critical ReviewsTM in Therapeutic Drug Carrier Systems, 36(2):137–181 (2019)
Kicamn, A. Pharmacology of anabolic steroids. British Journal of Pharmacology (2008) 154, 502–521. DOI: 10.1038/bjp.2008.165
Lockner, D. Treatment of Refractory Anemias with Methenolone. Acta Med Scand 205: 97-101, 1979
AHMED, S. F. et al. Randomized, crossover comparison study of the short-term effect of oral testosterone undecanoate and intramuscular testosterone depot on linear growth and serum bone alkaline phosphatase. Journal of Pediatric Endocrinology and Metabolism, v. 17, n. 7, p. 941-950, 2004.
BEHRE, Hermann M.; NIESCHLAG, Eberhard. Comparative pharmacokinetics of testosterone esters. In: Testosterone: Action-Deficiency-Substitution. Berlin, Heidelberg: Springer Berlin Heidelberg, 1998. p. 329-348.
SOLHEIM, Sara Amalie et al. An intramuscular injection of mixed testosterone esters does not acutely enhance strength and power in recreationally active young men. Frontiers in Physiology, v. 11, p. 563620, 2020.
CONWAY, Ann J. et al. Randomized clinical trial of testosterone replacement therapy in hypogonadal men. International journal of andrology, v. 11, n. 4, p. 247-264, 1988.
CONWAY, Ann J. et al. Use, misuse and abuse of androgens: The Endocrine Society of Australia consensus guidelines for androgen prescribing. Medical Journal of Australia, v. 172, n. 5, p. 220-224, 2000.
CANTRILL, Judith Anne et al. Which testosterone replacement therapy?. Clinical endocrinology, v. 21, n. 2, p. 97-107, 1984.
Durateston: solução injetável. Responsável técnico: Viviane L. Santiago Ferreira CRF-ES no 5139. São Paulo: Aspen Pharma Indústria Farmacêutica Ltda., 02/06/2020. Bula de remédio.
Nebido: solução injetável. São Paulo: Bayer S.A., 13/08/2009. Bula de remédio.

Comentários