NAC, glicina e taurina
no estresse oxidativo
Acesso rápido
Síntese endógena
NAC + glicina
Benefícios em adultos mais velhos
O fenômeno do roubo da glicose
Efeitos no DM2
Mecanismo de ação
Indivíduos imunossuprimidos
Outros efeitos metabólicos
Adultos saudáveis
Covid-19
Taurina e estresse oxidativo
Efeitos antioxidantes
Tampão mitocondrial
Taurina e glutationa
Suplementação com NAC, glicina e taurina
Conteúdos relacionados

A glutationa (GSH) é o mais abundante antioxidante sintetizado endogenamente e está presente na maioria das células, especialmente no fígado. Suas funções abrangem resposta imunológica adequada, síntese de ácidos nucleicos e, principalmente, neutralização das espécies reativas de oxigênio.
Espécies reativas de oxigênio (EROs) são substâncias altamente reativas produzidas naturalmente pelo organismo a partir dos processos metabólicos. Em condições ideais, o corpo tem capacidade de neutralizar as EROs e de manter a homeostase. Entretanto, quando há acúmulo dessas substâncias, o organismo pode não conseguir neutralizá-las de maneira eficiente, caracterizando o estresse oxidativo. Envelhecimento, tabagismo, dieta inadequada nutricionalmente, sedentarismo, inflamação, síndrome metabólica e outras condições podem contribuir para que isso ocorra.
Síntese endógena
O GSH é um tripeptídeo (γ-glutamil-cisteinil-glicina) sintetizado pela adição sequencial do aminoácido cisteína ao aminoácido glutamato, seguida pela adição de glicina. O grupo sulfidrila (-SH) presente na estrutura química da cisteína é o principal responsável pela função neutralizadora da glutationa.
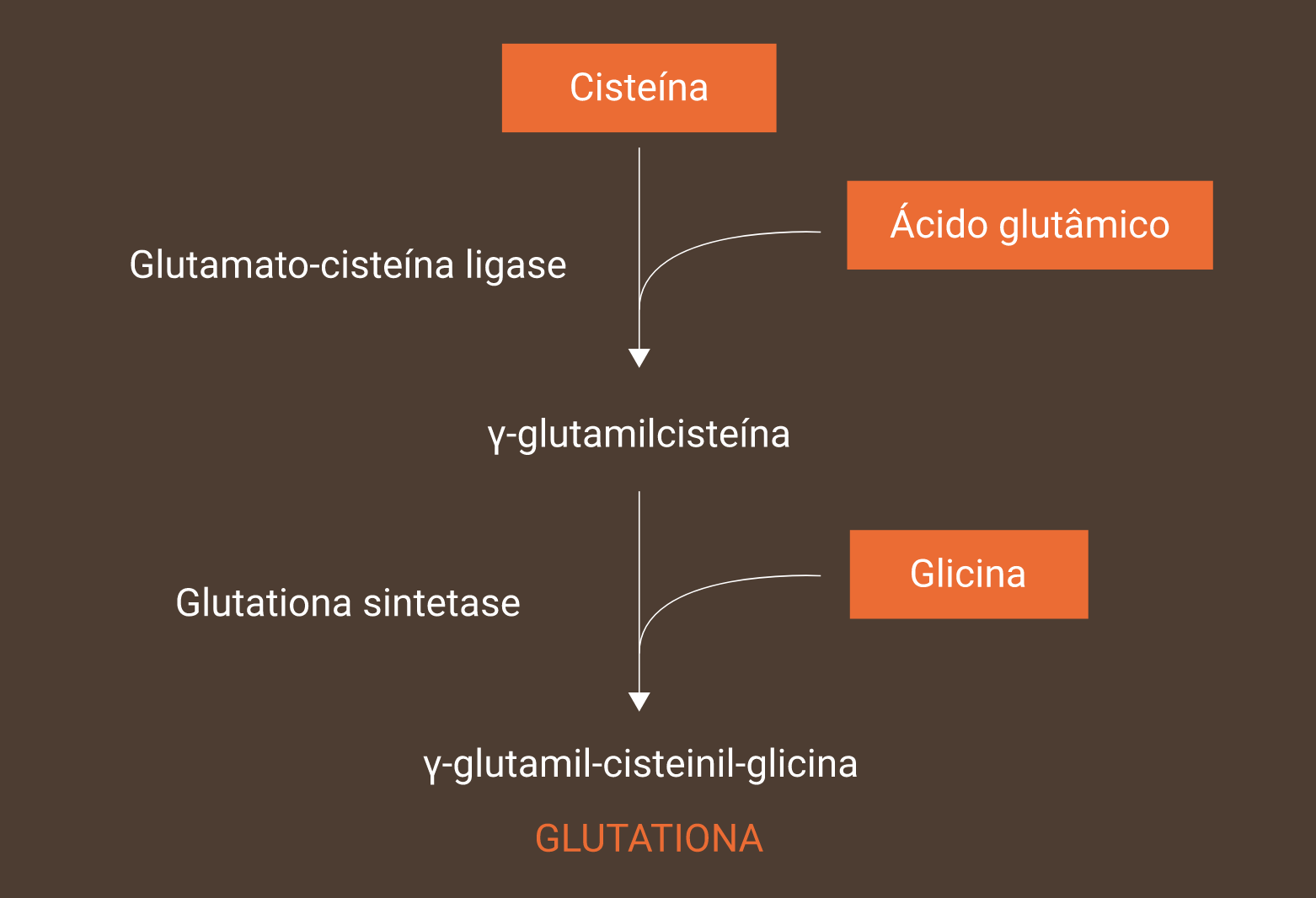
A síntese de glutationa é um processo de 2 etapas. A primeira etapa envolve a adição de cisteína e ácido glutâmico para formar o intermediário γ-glutamilcisteína. Na segunda etapa, a glicina é adicionada para formar a glutationa (γ-glutamil–cisteinil–glicina).
Algumas doenças caracterizadas por inflamação de baixo grau e/ou aumento da geração de EROs podem diminuir a síntese de GSH, como diabetes mellitus (DM), doenças cardiovasculares (DCV) e autoimunes.
No envelhecimento, a produção de glutationa também se mostra diminuída. Corrigir possíveis deficiências de glutationa a partir da sua suplementação não é tão simples, uma vez que a substância é digerida no intestino. Em contrapartida, alternativas que envolvem o uso de seus precursores se mostram bastante eficientes.

N-acetilcisteína, popularmente conhecida como NAC, é um derivado da cisteína e precursor de GSH. O NAC não modula apenas o estresse oxidativo, mas também outros processos fisiopatológicos como disfunção mitocondrial, apoptose e inflamação, e também apresenta efeitos indiretos em neurotransmissores como no glutamato e na dopamina. Devido às suas ações mucolíticas, a N-acetilcisteína também é comumente utilizada como tratamento em doenças respiratórias.
A glicina (Gli) é um aminoácido que compõe proteínas importantes e desempenha um papel fundamental na síntese de substâncias como creatina, nucleotídeos e GSH. Além disso, também atua como um neurotransmissor, modula a atividade neuronal no sistema nervoso central (SNC) e está envolvida na síntese de colágeno e regeneração tecidual.
Conforme já mencionado, a NAC e a Gli são precursores de glutationa e, por esse motivo, são consideradas potentes antioxidantes. Dessa forma, a suplementação conjunta das duas substâncias vem sendo alvo de pesquisas e os resultados são promissores. A essa junção, comumente dá-se o nome de GliNAC. Confira abaixo um compilado dos principais achados científicos.
Benefícios em adultos mais velhos
Um ensaio clínico randomizado investigou o efeito da suplementação de GliNAC nas concentrações de GSH, estresse oxidativo elevado (OxS), oxidação de ácidos graxos mitocondrial (MFO), resistência à insulina (RI), inflamação, função endotelial, função física e composição corporal. Participaram da pesquisa 24 adultos mais velhos com sobrepeso (idade ~70 anos) e 14 adultos para servir de grupo de comparação (idade ~25 anos).
Os adultos mais velhos receberam GliNAC (1,31mmol/kg/dia de glicina e 0,83mmol/kg/dia de NAC) – grupo OAG – ou placebo (alanina) – grupo OP – por 16 semanas, enquanto os adultos jovens receberam GliNAC por 2 semanas – grupo YA.
Ao comparar os grupos mais velhos com os adultos jovens, os primeiros apresentaram concentrações de GSH 66% menores, e também foi observada expressão diminuída de enzimas de síntese de glutationa. Após 2 semanas de suplementação, observou-se aumento de 121% nas concentrações de GSH e de 164% após 16 semanas, não diferindo dos níveis do grupo YA.
As concentrações de TBARS – indicador de OxS – foram 424% e 421% maiores nos grupos OAG e OP, respectivamente, na linha de base. Após 2 semanas, houve redução de 42% nesses valores e, após 16 semanas, de 72%, também não diferindo do grupo YA. Houve melhora em MFO (após 2 semanas: 29% maior; após 16 semanas: 78% maior), na expressão muscular de reguladores mitocondriais da biogênese e metabolismo energético e diminuição de citocinas pró-inflamatórias (IL-6 e TNFα), glicemia em jejum e RI.
Além disso, ao final do estudo, houve aumento da velocidade de marcha no grupo suplementado para níveis não diferentes de YA na linha de base e aumento da força muscular das extremidades superiores e inferiores. Os autores pontuaram que a suplementação de GliNAC em adultos mais velhos melhorou características do envelhecimento, como disfunção mitocondrial, inflamação crônica e anormalidades nos metabolismos energético e glicolítico.
O fenômeno do roubo da glicose
Uma consideração importante acerca dos efeitos do GliNAC em indicadores glicêmicos envolve o “fenômeno do roubo da glicose”, que pode ser o responsável pelo declínio cognitivo em idosos. Com o envelhecimento, é comum que haja diminuição de MFO, levando ao aumento do uso de glicose pelos tecidos. A correção da deficiência de GSH observada após a suplementação com GliNAC leva órgãos não cerebrais a utilizar novamente ácidos graxos para produzir energia, diminuindo o consumo de glicose. Isso leva a uma queda na oxidação glicolítica e, dessa forma, mais glicose está disponível para o cérebro. Essas alterações podem ser observadas por melhoras no desempenho cognitivo. O fato de pacientes com comprometimento cognitivo mostrarem diminuição da captação de glicose cerebral dá forças a essa suposição dos autores, bem como a correção nos valores do fator neurotrófico derivado do cérebro (BDNF) – um biomarcador da memória de longo prazo – após a suplementação de GliNAC.
Efeitos no DM2
De acordo com a literatura, pacientes com diabetes mellitus tipo 2 (DM2) apresentam deficiência de glutationa, pois há redução da disponibilidade dos aminoácidos precursores de GSH – glicina e cisteína, mas não ácido glutâmico. A suplementação desses nutrientes por 2 semanas mostrou corrigir a síntese prejudicada e diminuiu a OxS.
Nesse sentido, um estudo foi realizado com um subgrupo de dez adultos portadores de DM2 mal controlada que receberam suplementação de GliNAC (100mg/kg/dia de glicina e 100mg/kg/dia de NAC) ou placebo por 14 dias. Os dados foram comparados a um grupo controle, que não tinha diagnóstico de DM2 e não recebeu intervenção.
Na linha de base, os participantes diabéticos apresentaram 36% menos MFO (p=0,0006) e 106% maior oxidação de glicose mitocondrial (MGO) (p=0,008) em comparação aos controles. A suplementação de GliNAC foi associada a um aumento de 30% na MFO (p=0,0009) e a uma diminuição de 47% no MGO (p=0,001).
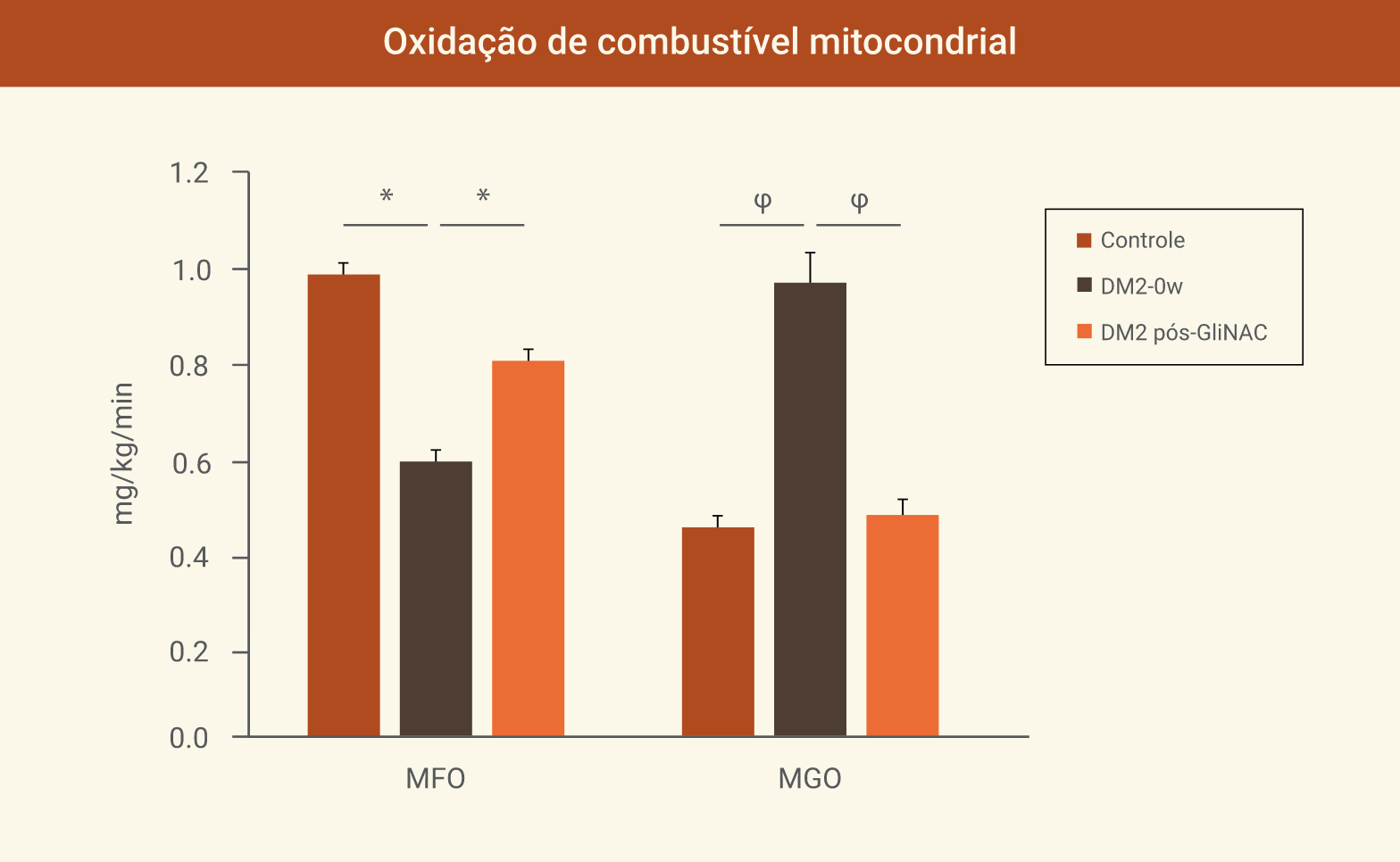
A suplementação com GliNAC melhorou a oxidação de combustível mitocondrial prejudicada em pacientes com DM2. DM2: diabetes tipo 2; MFO: oxidação de ácidos graxos mitocondriais; MGO: oxidação de glicose mitocondrial; DM2-0w: pacientes com DM2 antes da suplementação com GliNAC; DM2 pós-GliNAC: pacientes com DM2 2 semanas após a suplementação com GliNAC. ∗p<0,001; φ: p<0,01 (Sekhar, 2022).
Em jejum, os indivíduos com DM2 apresentaram concentrações 103%, 160% e 76% maiores de glicose plasmática (p<0,0001), insulina (p=0,0002) e AGL (p=0,015), respectivamente, e resistência à insulina 425% maior (p=0,0002) em comparação aos controles. Após a suplementação, houve redução significativa de 19% (p=0,0006) na insulina, 25% (p=0,004) em ácidos graxos livres e 22% (p=0,006) na RI. Os pesquisadores destacaram que, após interrupção da suplementação, houve uma perda dos benefícios observados.
Mecanismo de ação
Algumas razões podem explicar a melhora na RI com a suplementação de GliNAC. A resistência à insulina está associada à disfunção mitocondrial, níveis elevados de ácidos graxos livres e aumento de OxS, parâmetros que melhoraram após a intervenção. Em uma pesquisa com camundongos idosos, o mesmo grupo de pesquisa observou respostas mais altas de insulina e glicose, além de indicativos de atividade aumentada das células β e RI (eliminação prejudicada de glicose estimulada por insulina).
Quando os animais receberam GliNAC, sua eliminação de glicose estimulada por insulina melhorou para níveis observados em camundongos jovens. Ou seja, houve melhora na sensibilidade à insulina e, portanto, menos insulina foi necessária para eliminação de glicose, aliviando o estresse nas células β.
Indivíduos imunossuprimidos
Um grupo de pesquisadores realizou um estudo piloto com indivíduos mais velhos portadores de HIV e verificaram que a deficiência de GSH que ocorre nessa população se dá pela síntese diminuída ocasionada pela deficiência dos aminoácidos precursores, e que a suplementação de GliNAC por duas semanas melhorou a síntese de GSH eritrocitária, suas concentrações, a força muscular de preensão, a oxidação de combustível mitocondrial e diminuiu a inflamação.
Com a premissa de que a deficiência de glutationa nesses indivíduos está associada ao seu envelhecimento prematuro e que a sua suplementação poderia reverter essas condições, um ensaio clínico aberto com oito indivíduos portadores de HIV – pareados com oito controles não infectados – receberam GliNAC (glicina 1,31mmol/kg/d e NAC 0,83mmol/kg/d) por 12 semanas e foram estudados na linha de base, após 12 semanas de intervenção e 8 semanas após o término da suplementação.
O grupo experimental apresentava deficiência de GSH no músculo e eritrócitos, além de OxS significativamente maior na linha de base em comparação aos controles. A suplementação de GliNAC por 12 semanas aumentou o GSH muscular em 340% e o GSH eritrocitário em 46% e diminuiu o TBARS em 85%.
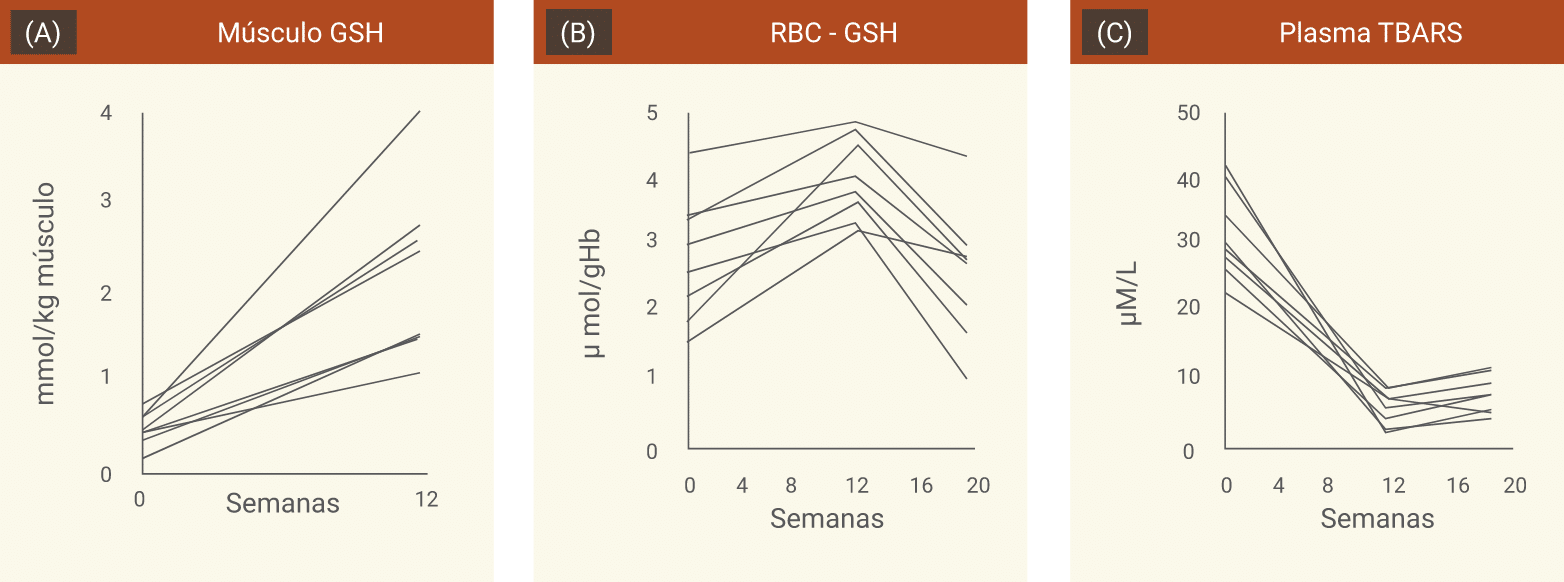
Dados individuais dos participantes mostrando o efeito da suplementação de GliNAC por 12 semanas e 8 semanas de abstinência. A e B: concentrações totais de GSH no músculo e eritrócitos, respectivamente e (C) concentrações plasmáticas de TBARS (Kumar et al., 2020).
Ainda na linha de base, os indivíduos imunossuprimidos apresentaram menor MFO e maiores MGO, glicemia de jejum, insulina e RI, com melhora significativa nesses parâmetros após a suplementação.
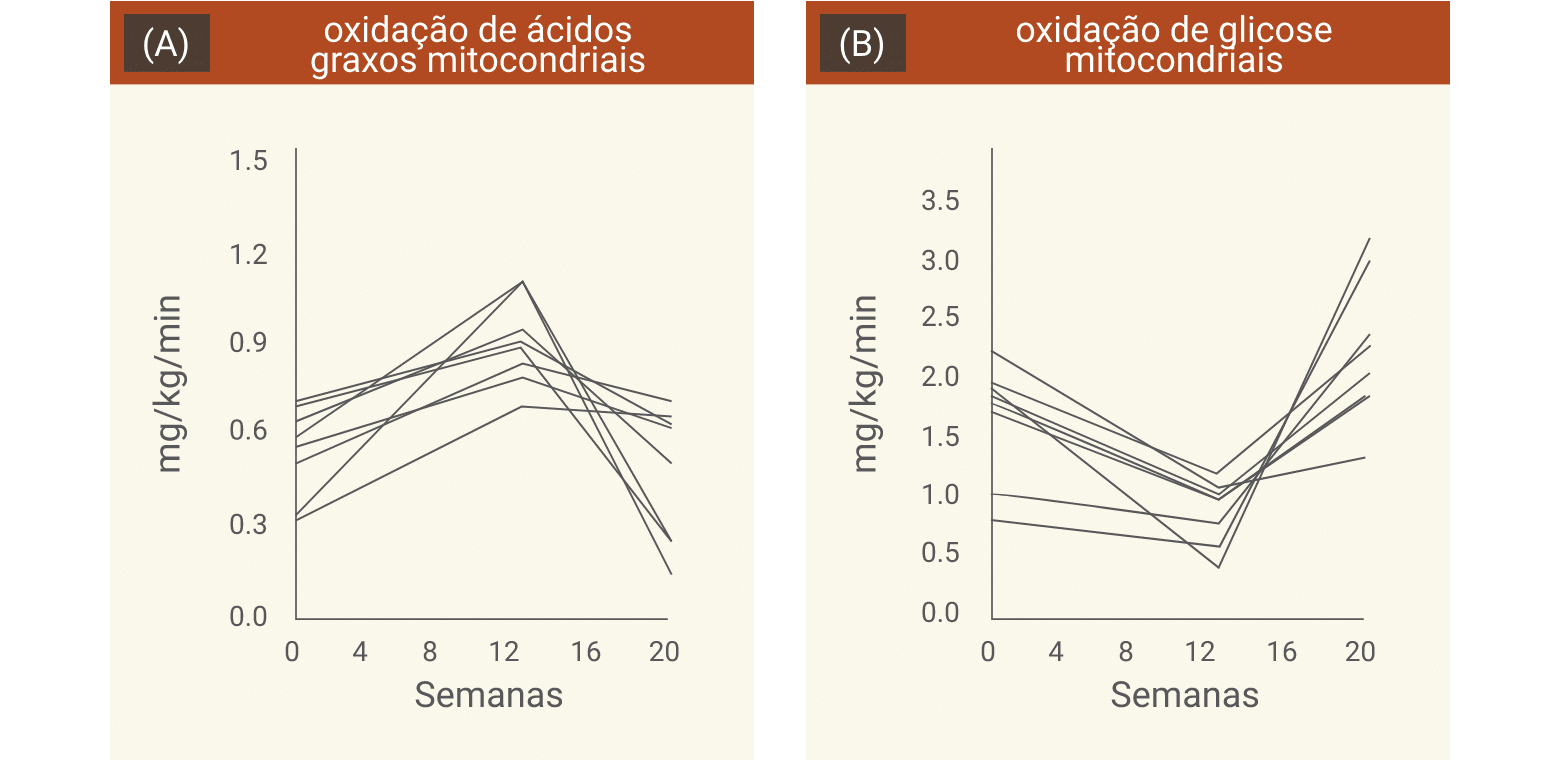
Dados individuais dos participantes mostrando oxidação de ácidos graxos mitocondriais em jejum (A) e oxidação de glicose (B) (Kumar et al., 2020).
Citocinas pró-inflamatórias também estavam mais altas nessas pessoas na linha de base, com diminuição significativa após a intervenção.
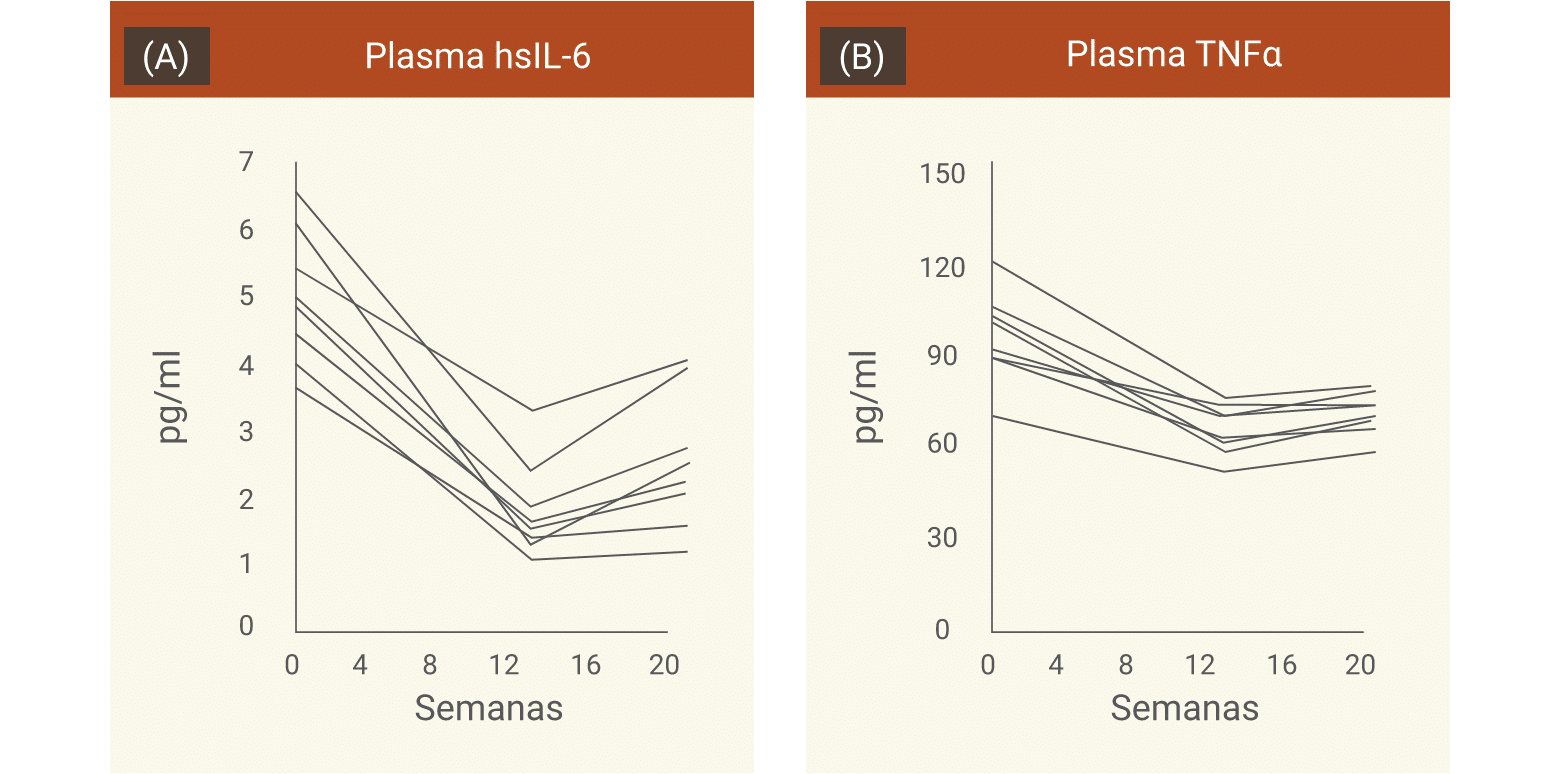
Dados individuais dos participantes mostrando concentrações plasmáticas de (A) interleucina 6 (IL-6); (B) fator de necrose tumoral alfa (TNFα) (Kumar et al., 2020).
Resultados adicionais incluem: melhora na disfunção endotelial, na velocidade de marcha, força de preensão do antebraço e nos níveis de BDNF plasmático. Ainda, houve diminuição do IMC, da gordura corporal total, da circunferência da cintura e da relação cintura/quadril.
Embora o estudo não tenha se concentrado na doença hepática gordurosa não alcoólica (DHGNA), a imagem hepática revelou DHGNA subclínica em 2 de 8 participantes estudados, e a fração de gordura do fígado diminuiu em 40% com a suplementação de GliNAC nesses 2 participantes. Os pesquisadores sugerem que a oxidação prejudicada de ácidos graxos mitocondriais promove o armazenamento de gordura, e que a suplementação de GliNAC pode reduzir a gordura corporal total, melhorando a MFO.
Entretanto, muitas das melhorias observadas no estudo retrocederam após a interrupção da suplementação por 8 semanas.
Outros efeitos metabólicos
Devido às suas ações que envolvem o metabolismo energético, a inflamação e parâmetros glicêmicos, o uso da glicina com a N-acetilcisteína – GliNAC – abrange várias situações, inclusive preventivas.
Adultos saudáveis
Um ensaio clínico randomizado controlado objetivou avaliar a eficácia e segurança de uma suplementação de GliNAC em adultos mais velhos saudáveis (60-85 anos). Um grupo de 20 voluntários jovens saudáveis (idade ~31,7 anos) foi recrutado como comparação de resultados. Os adultos mais velhos foram randomizados em 4 grupos: grupo placebo, grupo 2,4g de ativos (1,2g NAC + 1,2g glicina), grupo 4,8g de ativos (2,4g NAC + 2,4g glicina) ou grupo 7,2 g de ativos (3,6g NAC + 3,6g glicina).
Os participantes mais velhos apresentaram níveis mais altos de malondialdeído (MDA). Apesar de níveis normais de GSH, os níveis de GSH oxidada (GSSG) estavam significativamente aumentados, levando a uma menor proporção de GSH reduzida/oxidada.
Os indivíduos que receberam 4,8g e 7,8g de ativos, após 2 semanas de suplementação, mostraram um aumento de 10,5% nos níveis de GSH. Além disso, observou-se efeito de aumento nos níveis de glicina em comparação com a linha de base para níveis perto da mediana dos indivíduos jovens.
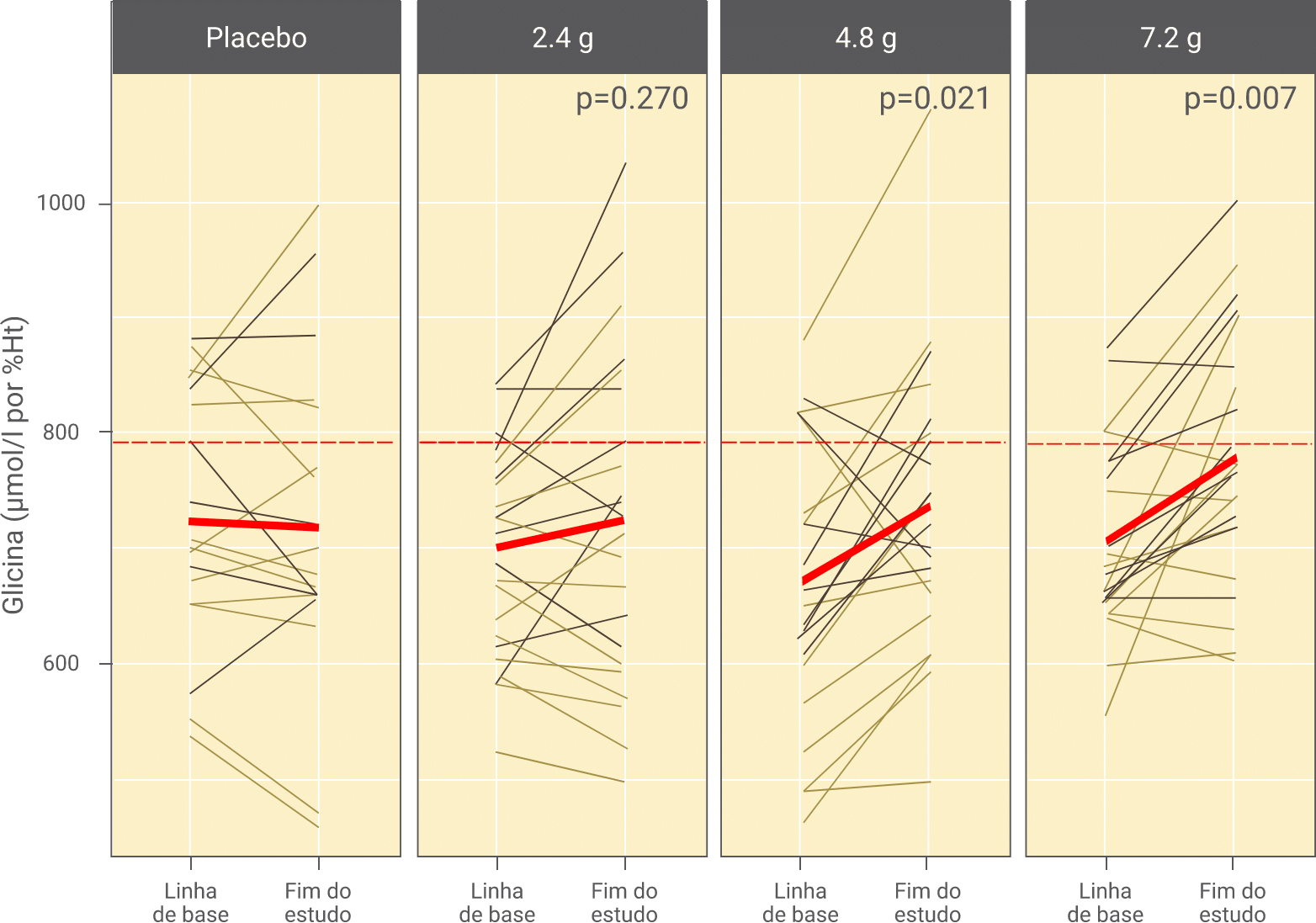
Efeitos da ingestão diária de placebo ou doses diferentes de GliNAC nos níveis de glicina no sangue total em uma subpopulação de adultos mais velhos (excluindo o grupo acima do terceiro quartil). Os níveis de glicina foram comparados antes e após as 2 semanas de tratamento em amostras coletadas antes da dosagem com GliNAC. As linhas tracejadas vermelhas representam a mediana dos adultos jovens. p: valor de p, modelo misto linear testando alterações intraindividuais da linha de base ao fim do estudo dentro de cada grupo de dose e do grupo placebo (Lizzo et al., 2022).
Os autores evidenciam que, mesmo nesses indivíduos que representam o envelhecimento saudável, vários marcadores relacionados ao dano oxidativo diferem dos jovens, sugerindo um ambiente sistêmico pró-oxidativo nessa faixa etária.
Covid-19
No covid-19 foi observado em um estudo que as concentrações de GSH eritrocitária são 60,2%, 74,7% e 48,3% menores em humanos jovens (21-40 anos), de meia-idade (41-60 anos) e mais velhos (≥60 anos) em comparação aos seus pares controles não infectados.
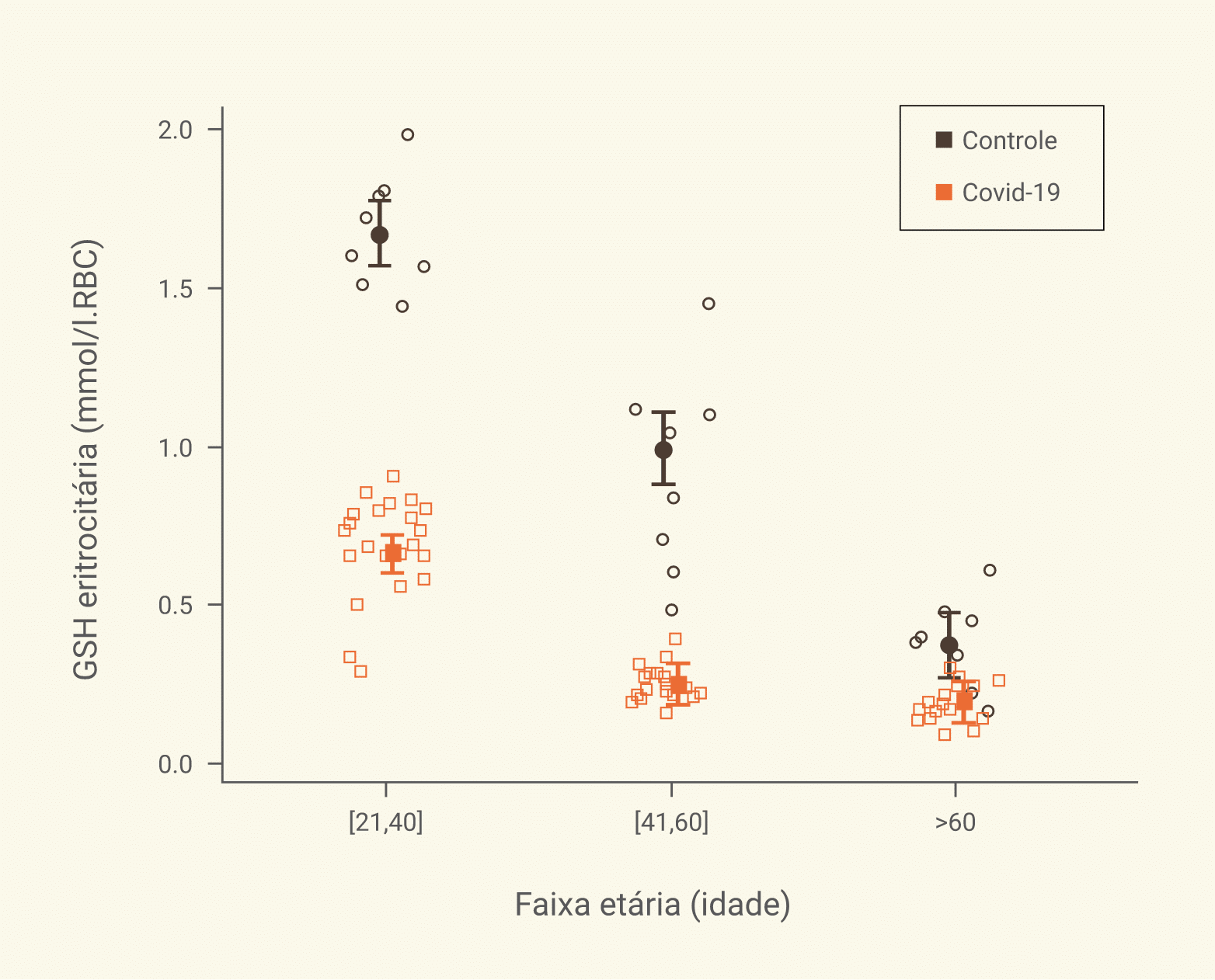
Concentrações intracelulares reduzidas de glutationa por idade e coorte (pacientes com COVID-19 vs. controles não infectados) com médias estimadas de regressão (IC de 95%) ajustando para coorte, idade, grupo e sexo (Kumar et al., 2021).
Os níveis de TBARS, em comparação aos controles, foram 203% maiores nos pacientes acometidos pela doença. Ao analisar de acordo com a faixa etária, aqueles com covid-19 apresentaram concentrações 654%, 1007% e 70,6% maiores de TBARS em humanos jovens (21-40 anos), de meia-idade (41-60 anos) e mais velhos (≥60 anos), respectivamente, sugerindo OxS grave e elevado nessa condição.
Esses dados mostram que, apesar da magnitude dos efeitos aumentar com a idade, a deficiência de glutationa também é vista nos mais jovens, especialmente em situações de OxS elevado e aumento de danos oxidantes.

A taurina (Tau) é um aminoácido abundantemente encontrado em tecidos como a retina, o músculo esquelético e o fígado, exercendo muitas atividades fisiológicas, principalmente no coração e cérebro. Sua biossíntese é dependente do metabolismo da cisteína/metionina, e a capacidade do ser humano de produzi-la começa a declinar na idade adulta, atingindo suas concentrações mais baixas em idosos e em condições patológicas.
A alta concentração de taurina e seu transportador em linfócitos evidencia seu envolvimento na defesa contra o estresse oxidativo. Por outro lado, baixos níveis séricos têm sido associados a patologias mediadas pelo estresse oxidativo, como distúrbios hepáticos, cardiomiopatia, fibrose cística, doença de Alzheimer e degeneração da retina.
Efeitos antioxidantes
Já houve especulações de que a Tau aumenta a atividade de enzimas antioxidantes (superóxido dismutase-SOD, catalase-CAT, glutationa peroxidase-GPx, glutationa redutase-GR), preservando os níveis redox e os estoques de GSH. A taurina tem a capacidade de neutralizar o ácido hipocloroso, um oxidante extremamente tóxico produzido pelos leucócitos no processo inflamatório em humanos. Sua ação citoprotetora é baseada também em sua capacidade de desintoxicar peróxido de hidrogênio, radicais hidroxila e NO.
De acordo com as pesquisas, os fenótipos deficientes em Tau são caracterizados por deficiências no crescimento, metabolismo energético e função do músculo esquelético, cardiopatia e degeneração da retina. Também foi demonstrado que o desempenho de camundongos transgênicos sem o transportador de taurina (TauT) foi comprometido, com geração de ROS significativamente aumentada e anormalidades musculares.
Estudos in vitro com cardiomiócitos deficientes em Tau mostraram que a produção excessiva de ROS foi suprimida após a adição de Tau ao meio. Em condições de estresse, a estabilização mitocondrial por taurina mantém a homeostase e o equilíbrio redox, diminuindo o vazamento de ROS produzidos dentro das mitocôndrias.
Uma pesquisa investigou os efeitos da suplementação de taurina (1,6g/dia) ou placebo (amido) por 16 semanas em 24 mulheres (idade ~61,4 anos). Como resultado, os níveis de SOD aumentaram significativamente no grupo suplementado com Tau (GTAU) (η2=0,56; p<0,001) em comparação ao placebo (GC). No GC, o MDA aumentou após a intervenção em comparação ao GTAU (p=0,010), enquanto o segundo não apresentou alterações, sugerindo que a taurina preveniu o aumento da peroxidação lipídica.
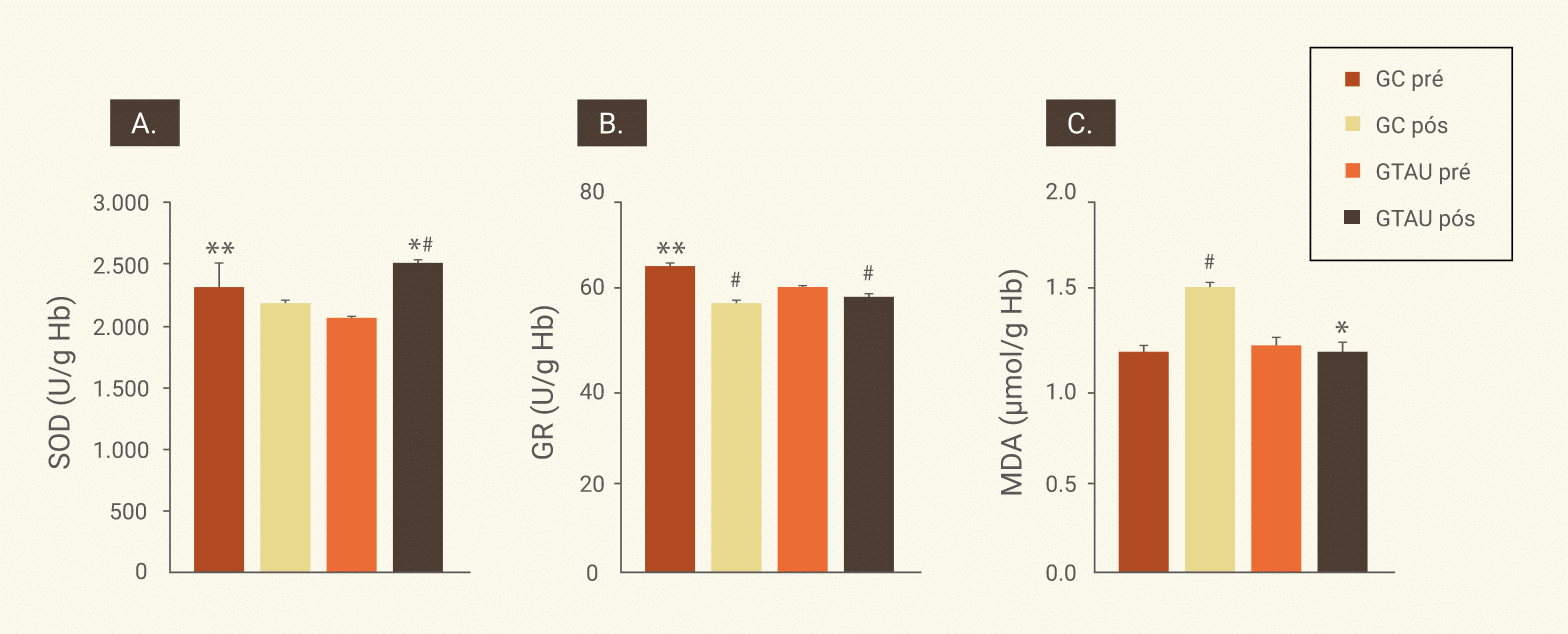
Níveis de marcadores de estresse oxidativo pré e pós-intervenção. GC: grupo controle; GTAU: grupo taurina. A. SOD: superóxido dismutase; B. GR: glutationa redutase; C. MDA: malondialdeído; Hb: homoglobina. Valores expressos como média ± DP. **Diferença entre os grupos pré-intervenção. *Diferença entre os grupos pós-intervenção. #Diferença dentro dos grupos pós-intervenção, por análise de variância bidirecional, modelo misto de medidas repetidas (p<0,05). SOD: η2 =0,56; MDA: η2 =0,67.
Devido aos efeitos antioxidantes, ações na função vascular e endotelial, contratilidade cardíaca, metabolismo glicolítico e lipídico também já foram documentados. Em homens idosos, a suplementação de Tau parece diminuir o risco cardiometabólico. Já em mulheres mais velhas, houve diminuição dos níveis de SOD plasmáticos.
Tampão mitocondrial
Uma competência da taurina investigada é a de tampão de pH na matriz mitocondrial. Um pH ligeiramente alcalino é um ambiente ideal para a beta-oxidação de ácidos graxos e, como a oxidação é muito dependente do pH, a existência de um tampão de pH parece necessária para aumentar a capacidade de armazenamento energético. Assim, a Tau atua como tampão mitocondrial, havendo equilíbrio termodinâmico entre os pares redox NADH/NAD+ e GSH/GSSG.
Há evidências de que a suplementação de taurina protege contra a disfunção mitocondrial. A exposição de cardiomiócitos a um meio contendo β-alanina – antagonista da Tau – levou a um aumento do estresse oxidativo mitocondrial e oxidação de GSH. Outro marcador de estresse oxidativo, o estado redox da glutationa (relação glutationa reduzida/glutationa oxidada), caiu 43% após 48h de tratamento com β-alanina, mas permaneceu inalterado após uma incubação com meio sem β-alanina, contendo tanto taurina quanto β-alanina ou contendo apenas taurina.
Dois marcadores de estresse oxidativo mitocondrial – atividade de aconitase e succinato desidrogenase – foram determinados em células tratadas com β-alanina, co-tratadas com taurina e β-alanina, tratadas com taurina e não tratadas. O tratamento com β-alanina não teve efeito na atividade da succinato desidrogenase, mas reduziu a atividade da aconitase em 45%. Em contraste, a atividade da aconitase nas células tratadas com taurina e co-tratadas com taurina e β-alanina foi indistinguível da das células controle, sugerindo efeito protetor da Tau à ação da β-alanina.
Desse modo, a taurina serve como um regulador da síntese de proteínas mitocondriais, aumentando assim a atividade da cadeia de transporte de elétrons e protegendo as mitocôndrias contra a geração excessiva de superóxido.
Taurina e glutationa
Pesquisadores investigaram os efeitos da suplementação de taurina em tecidos do cristalino em um modelo in vivo de estresse oxidativo, induzido pela depleção de GSH a partir de sulfoximina (BSO). Coelhos brancos foram divididos em 4 grupos: (1) controle; (2) BSO; (3) BSO + Tau e (4) Tau.
O tratamento com BSO reduziu significativamente os níveis de glutationa. Quando os animais foram alimentados com taurina simultaneamente ao BSO, os níveis de GSH foram restaurados. BSO também reduziu a relação GSH/GSSG, e a taurina reverteu esse efeito. O uso de BSO também aumentou o nível de MDA, mas quando os animais foram alimentados com Tau simultaneamente ao BSO, o nível de MDA foi restaurado.
Esses resultados indicam que a suplementação de taurina in vivo repõe os níveis de GSH e reduz indicadores de peroxidação lipídica.

Tendo em vista a ampla gama de condições que diminuem a síntese de GSH, fórmulas com precursores de glutationa e ingredientes que atuam em sinergia podem ser uma alternativa para a manutenção da capacidade antioxidante do organismo, favorecendo a nutrição celular e a homeostase do corpo.
NAC+ glycine + taurine é uma fórmula vegana feita com matéria-prima de alta qualidade, contendo 1000mg de glicina, 600mg de L-cisteína (na forma de NAC) e 500mg de taurina. Uma forma altamente eficaz de fornecer os aminoácidos necessários para a síntese da glutationa.
IMPORTANTE
Este material é de apoio técnico para prescritores e é proibida a sua divulgação para consumidores, nos termos do item 5.14 da RDC 67/2007.
Conteúdos relacionados
A CIESLIK, Katarzyna et al. Improved Cardiovascular Function in Old Mice After N-Acetyl Cysteine and Glycine Supplemented Diet: inflammation and mitochondrial factors. The Journals Of Gerontology: Series A, v. 73, n. 9, p. 1167-1177, 2018.
ABUD, Gabriela Ferreira et al. Taurine as a possible antiaging therapy: a controlled clinical trial on taurine antioxidant activity in women ages 55 to 70. Nutrition, v. 101, 2022.
AGUAYO-CERÓN, Karla Aidee et al. Glycine: the smallest anti-inflammatory micronutrient. International Journal Of Molecular Sciences, v. 24, n. 14, 2023.
BALIOU, Stella et al. Protective role of taurine against oxidative stress (Review). Molecular Medicine Reports, v. 24, n. 2, 2021.
CASTELLI, Vanessa et al. Taurine and oxidative stress in retinal health and disease. Cns Neuroscience & Therapeutics, v. 27, n. 4, p. 403-412, 2021.
CHUPEL, Matheus Uba et al. Exercise and taurine in inflammation, cognition, and peripheral markers of blood-brain barrier integrity in older women. Applied Physiology, Nutrition, And Metabolism, v. 43, n. 7, p. 733-741, 2018.
HANSEN, Svend Høime; GRUNNET, Niels. Taurine, Glutathione and Bioenergetics. Advances In Experimental Medicine And Biology, p. 3-12, 2013.
HERZENBERG, Leonore A. et al. Glutathione deficiency is associated with impaired survival in HIV disease. Proceedings Of The National Academy Of Sciences, v. 94, n. 5, p. 1967-1972, 1997.
JONG, Chian Ju; AZUMA, Junichi; SCHAFFER, Stephen. Mechanism underlying the antioxidant activity of taurine: prevention of mitochondrial oxidant production. Amino Acids, v. 42, n. 6, p. 2223-2232, 2011.
JONG, Chian Ju; SANDAL, Priyanka; SCHAFFER, Stephen W. The Role of Taurine in Mitochondria Health: more than just an antioxidant. Molecules, v. 26, n. 16, 2021.
KUMAR, Premranjan et al. Severe Glutathione Deficiency, Oxidative Stress and Oxidant Damage in Adults Hospitalized with COVID-19: implications for glynac (glycine and n-acetylcysteine) supplementation. Antioxidants, v. 11, n. 1, 2021.
KUMAR, Premranjan et al. Supplementing Glycine and N-acetylcysteine (GlyNAC) in Aging HIV Patients Improves Oxidative Stress, Mitochondrial Dysfunction, Inflammation, Endothelial Dysfunction, Insulin Resistance, Genotoxicity, Strength, and Cognition: results of an open-label clinical trial. Biomedicines, v. 8, n. 10, 2020.
KUMAR, Premranjan et al. Supplementing Glycine and N-Acetylcysteine (GlyNAC) in Older Adults Improves Glutathione Deficiency, Oxidative Stress, Mitochondrial Dysfunction, Inflammation, Physical Function, and Aging Hallmarks: a randomized clinical trial. The Journals Of Gerontology: Series A, v. 78, n. 1, p. 75-89, 2022.
KUMAR, Premranjan; OSAHON, Ob W.; SEKHAR, Rajagopal V.. GlyNAC (Glycine and N-Acetylcysteine) Supplementation in Mice Increases Length of Life by Correcting Glutathione Deficiency, Oxidative Stress, Mitochondrial Dysfunction, Abnormalities in Mitophagy and Nutrient Sensing, and Genomic Damage. Nutrients, v. 14, n. 5, 2022.
LIZZO, Giulia et al. A Randomized Controlled Clinical Trial in Healthy Older Adults to Determine Efficacy of Glycine and N-Acetylcysteine Supplementation on Glutathione Redox Status and Oxidative Damage. Frontiers In Aging, v. 3, 2022.
NGUYEN, Dan et al. Effect of Increasing Glutathione With Cysteine and Glycine Supplementation on Mitochondrial Fuel Oxidation, Insulin Sensitivity, and Body Composition in Older HIV-Infected Patients. The Journal Of Clinical Endocrinology & Metabolism, v. 99, n. 1, p. 169-177, 2014.
NGUYEN, Dan et al. Impaired mitochondrial fatty acid oxidation and insulin resistance in aging: novel protective role of glutathione. Aging Cell, v. 12, n. 3, p. 415-425, 2013.
NGUYEN, Dan; JEAN, W Hsu; JAHOOR, Farook; RAJAGOPAL, V Sekhar. Effect of Increasing Glutathione With Cysteine and Glycine Supplementation on Mitochondrial Fuel Oxidation, Insulin Sensitivity, and Body Composition in Older HIV-Infected Patients. The Journal Of Clinical Endocrinology & Metabolism, v. 99, n. 1, p. 169-177, 2014.
OLIVEIRA, Max W.s. et al. Scavenging and antioxidant potential of physiological taurine concentrations against different reactive oxygen/nitrogen species. Pharmacological Reports, v. 62, n. 1, p. 185-193, 2010.
RAGHU, Ganesh et al. The Multifaceted Therapeutic Role of N-Acetylcysteine (NAC) in Disorders Characterized by Oxidative Stress. Current Neuropharmacology, v. 19, n. 8, p. 1202-1224, 2021.
ROSA, Flávia Troncon et al. Oxidative stress and inflammation in obesity after taurine supplementation: a double-blind, placebo-controlled study. European Journal Of Nutrition, v. 53, n. 3, p. 823-830, 2013.
SANTULLI, Gaetano et al. Functional Role of Taurine in Aging and Cardiovascular Health: an updated overview. Nutrients, v. 15, n. 19, 2023.
SEKHAR, Rajagopal V et al. Deficient synthesis of glutathione underlies oxidative stress in aging and can be corrected by dietary cysteine and glycine supplementation. The American Journal Of Clinical Nutrition, v. 94, n. 3, p. 847-853, 2011.
SEKHAR, Rajagopal V. et al. Glutathione Synthesis Is Diminished in Patients With Uncontrolled Diabetes and Restored by Dietary Supplementation With Cysteine and Glycine. Diabetes Care, v. 34, n. 1, p. 162-167, 2010.
SEKHAR, Rajagopal V.. GlyNAC (Glycine and N-Acetylcysteine) Supplementation Improves Impaired Mitochondrial Fuel Oxidation and Lowers Insulin Resistance in Patients with Type 2 Diabetes: results of a pilot study. Antioxidants, v. 11, n. 1, 2022.
SEVIN, G. et al. Taurine supplementation protects lens against glutathione depletion. European Review For Medical And Pharmacological Sciences, v. 25, n. 13, p. 4520-4526, 2021.
SURAI, Peter F.; EARLE-PAYNE, Katie; KIDD, Michael T.. Taurine as a Natural Antioxidant: from direct antioxidant effects to protective action in various toxicological models. Antioxidants, v. 10, n. 12, 2021.
XU, Xin et al. Glycine and N-Acetylcysteine (GlyNAC) Combined with Body Weight Support Treadmill Training Improved Spinal Cord and Skeletal Muscle Structure and Function in Rats with Spinal Cord Injury. Nutrients, v. 15, n. 21, 2023.






Pesquisa excelente e objetiva obrigado
Olá Dr Luiz, agradecemos imensamente seu feedback ♥ Um grande abraço, Essentia Group