Ácido α-lipoico injetável
Relevante potencial antioxidante, terapêutico e quelante no uso injetável
O que é o ácido α-lipoico?
Com propriedades antioxidantes conhecidas desde 1959, o ácido α-lipoico (ALA) apresenta resultados terapêuticos no alívio de sintomas relacionados a certas condições, como diabetes, Alzheimer, imperfeições cardiovasculares e neuromusculares — relacionados à idade —, ganho de peso devido ao consumo de medicamentos antipsicóticos e obesidade metabólica.
Normalmente encontrado nas mitocôndrias, o ácido α-lipoico participa de diversas funções enzimáticas, entre elas a quelação de metais. Enquanto em sua forma reduzida, o DHLA, é capaz de regenerar a vitamina E e a vitamina C ao serem oxidadas no organismo.
Apesar de ser encontrado no fígado e nos músculos esqueléticos de animais e humanos, e em alguns vegetais, como batata e brócolis, as quantidades produzidas naturalmente não são suficientes para suprir a energia necessária pela célula, necessitando a suplementação exógena. Otimizada através da administração por injetáveis, apresenta baixa biodisponibilidade por via oral.
Os suplementos nutricionais contendo ALA são tipicamente compostos pelo isômero óptico R-α-lipoico isolado ou por uma mistura racêmica de ácido R-α-lipoico e ácido S-α-lipoico, conforme demonstrado nas figuras estruturais químicas abaixo.
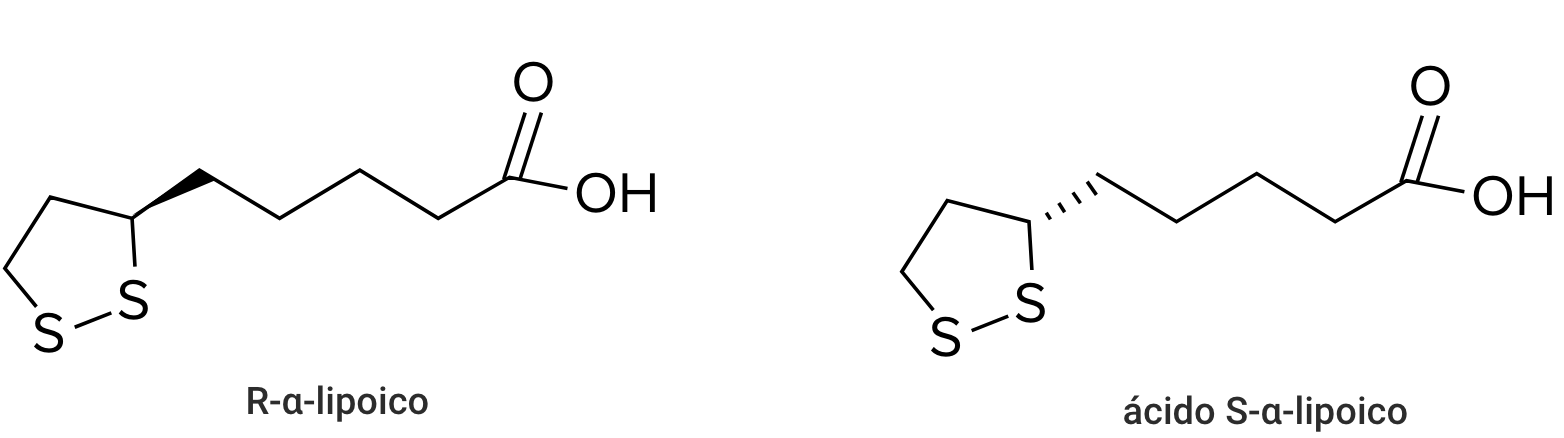
Figura 1: estruturas químicas das moléculas de ácido α-lipoico.
Potencial antioxidante
Em seu papel oxidativo, o ALA exerce uma ação direta doando elétrons para um pró-oxidante ou uma molécula oxidada, o que previne o estresse oxidativo. Espécies reativas de oxigênio (ROS) são moléculas reativas derivadas do subproduto natural do metabolismo do oxigênio e apresentam papéis significativos na homeostase e na sinalização celular. Elas são equilibradas por meio da presença de grupos antioxidantes, que podem ser enzimáticos (endógenos) ou não enzimáticos (exógenos). Quebrar esse equilíbrio com a superprodução de ROS, ou pela redução de antioxidantes, pode ser danoso e conduz ao estresse oxidativo.
Quando o estresse oxidativo ocorre, as células são sinalizadas e agem neutralizando os efeitos oxidantes, a fim de restaurar o equilíbrio redox, redefinindo parâmetros homeostáticos críticos. Essa atividade celular induz à ativação ao silenciamento de genes que codificam enzimas defensivas, fatores de transcrição e proteínas. De acordo com a teoria dos radicais livres, as ROS geradas por fatores endógenos, bem como fontes exógenas, geram danos ao DNA e acumulação de proteínas e lipídios, quando os mecanismos de defesa tornam-se fracos. Essas ROS também modulam a transdução de sinal e esses distúrbios causam danos nas organelas, mudanças na expressão gênica e alteração das respostas celulares, o que resulta no envelhecimento celular desordenado, conforme demonstrado na figura 2.
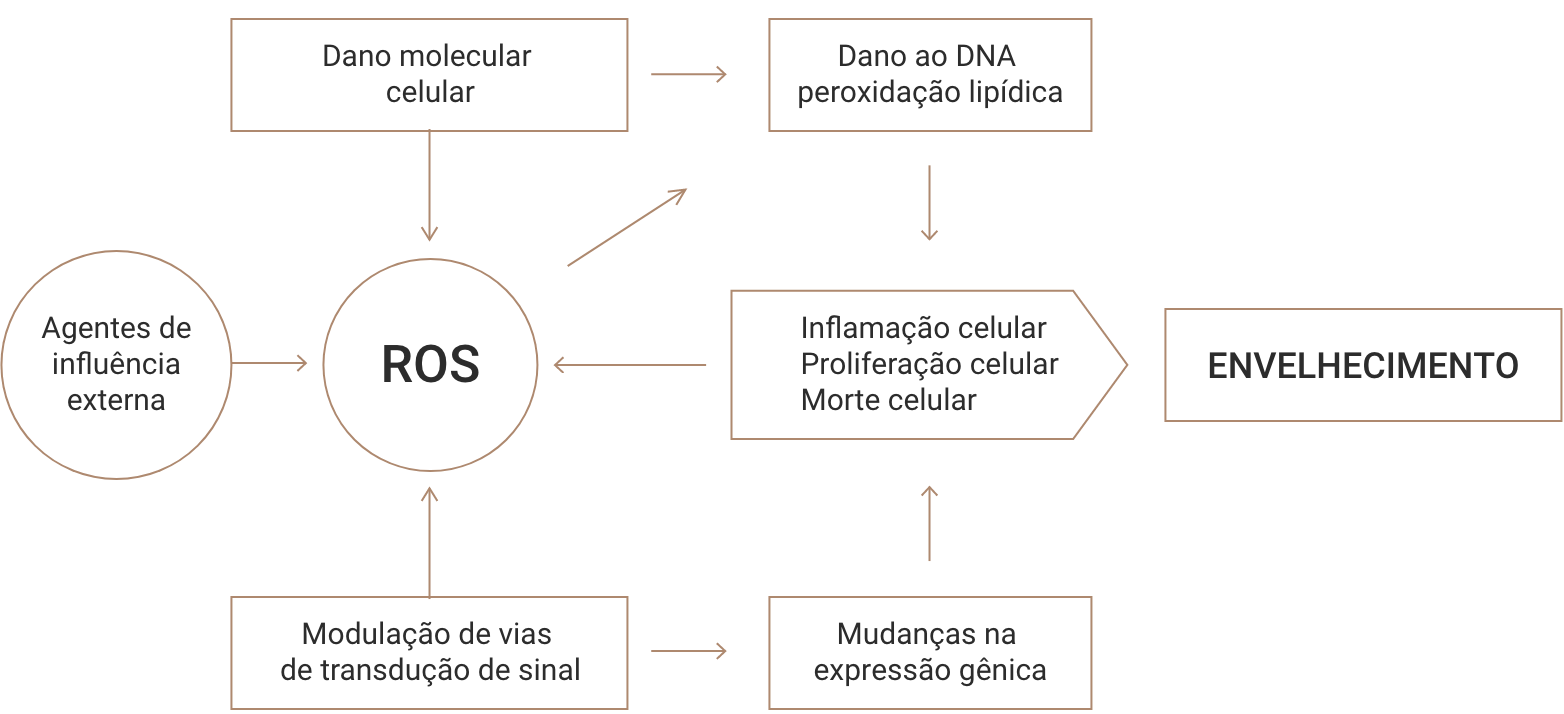
Figura 2: esquema didático representando o envelhecimento celular desordenado desencadeado pela ROS.
Apresentações disponíveis
Ácido α-lipoico 10mg/2mL – uso EV / IM / SC / ID
Ácido α-lipoico 100mg/5mL – uso EV / IM / SC / ID
Ácido α-lipoico 300mg/10mL – uso EV (exclusivo)
Ácido α-lipoico 600mg/Frasco 24mL – uso EV (exclusivo)
Indicações terapêuticas
 Ação antioxidante
Ação antioxidante
 Potencial terapêutico
Potencial terapêutico
 Aumento dos níveis de glutationa dentro das células
Aumento dos níveis de glutationa dentro das células
 Capacidade quelante de metais tóxicos
Capacidade quelante de metais tóxicos
Ação do ácido α-lipoico em diferentes condições:
Diabetes
A diabetes mellitus (DM) é definida por distúrbios no metabolismo de carboidratos, lipídios e proteínas. Reconhecida como um fator de risco para o desenvolvimento de diversas condições humanas, como:
• Aterosclerose
• Hipertensão
• Insuficiência cardíaca
• Infarto do miocárdio
• Dor neuropática
• Acidente vascular cerebral
Testes clínicos com infusão aguda de ácido α-lipoico comprovaram que a suplementação pode:
• Melhorar os sintomas neuropáticos positivos
• Contribuir na vasodilatação
• Aumentar a microcirculação em pacientes com polineuropatia diabética
• Ajudar na captação da glicose periférica
• Eliminar radicais livres
• Promover a regeneração da fibra muscular
Câncer
Nesse viés, o ácido α-lipoico foi administrado como um agente anticancerígeno, principalmente em estudos experimentais de diferentes tipos de células cancerígenas, e apresentou bons resultados. Uma das propostas de atuação do ALA é na ativação da via mitocondrial, responsável pela apoptose celular, por meio da capacidade de gerar espécies reativas de oxigênio, observada em células cancerígenas de cólon, mama e pulmão.
A suplementação contribui para:
• Bloqueio da via glicolítica, fazendo com que menos moléculas de lactato sejam geradas e melhorando o prognóstico do câncer
• Supressão da proliferação e do crescimento de células cancerígenas de tireoide por meio da ativação de AMPK
• Inibição da proliferação celular em células de câncer de pulmão, através da regulação negativa do EGFR
Alzheimer
Como uma condição neurodegenerativa crônica definida por alterações cognitivas, funcionais e comportamentais, o Alzheimer apresenta mecanismos como:
• Privação de dano sináptico no córtex cerebral e em áreas subcorticais
• Atrofia e degeneração celular das regiões afetadas
• Sintomas de inflamação ao redor das placas senis.
• Níveis aumentados de glutamato extracelular
Devido às suas propriedades antioxidantes e à sua capacidade de modular várias cascatas de sinalização, o ácido α-lipoico é utilizado como terapia alternativa para a DA. Resultados promissores provam que:
• Reprime o final da glicação avançada
• Protege e preserva neurônios hipocampais primários
• Aumenta a sobrevivência das células neuronais
• Ativa vias fosfoinositol-3 quinase (PI3K), PKC e ERK1/2
Efeitos adversos
Podem incluir náuseas, vômitos e vertigem em pacientes com neuropatia periférica. Infusões muito rápidas com diluições inadequadas podem causar embolia gordurosa e coagulopatia.
Contraindicações
Não é recomendada a administração de nenhum outro medicamento 30 minutos antes ou após a administração parenteral do ácido α-lipoico. Se necessário o uso de outro ativo, realizar a lavagem da via com 100mL de SF 0,9% antes da nova administração.
Vias de administração
Oral: a dose máxima tolerada em pacientes é de 1200 a 1800mg/dia, por mês.
Endovenosa: é recomendada a dose de 600mg (contudo, para a primeira administração, não recomenda-se exceder 250mg), utilizando bolsa de soro fisiológica de 250 ou 500ml. Para uma administração segura, sugere-se que a infusão seja de forma lenta, gotejando 5ml com 10mg por minuto.
Importante que os sinais vitais do paciente sejam acompanhados e documentados durante 30 minutos após a primeira infusão ou qualquer tratamento subsequente em que tenha ocorrido o aumento da dose. Para infusões de rotina, pode-se monitorar o paciente por no mínimo 15 minutos após a infusão.
IMPORTANTE
Este material é de apoio técnico para prescritores e é proibida a sua divulgação para consumidores, nos termos do item 5.14 da RDC 67/2007.
Reed, L.J.; DeBusk, B.G.; Gunsalus, I.C.; Hornberger, C.S. Crystalline α-lipoic acid: A catalytic agent associated with pyruvate dehydrogenase. Science 1951, 114, 93–94.
Salehi, B. et al. Insights on the Use of α-Lipoic Acid for Therapeutic Purposes. Biomolecules. 2019, 9, 356. DOI: 10.3390/biom9080356
Brufani, M. Figliola, R. (R)-α-lipoic acid oral liquid formulation: pharmacokinetic parameters and therapeutic efficacy. Acta Bio-medica: Atenei Parmensis. 2014, 2 p.108-115. PMID: 25245645.
Bock, E.; Schneeweiss, J. Ein Beitrag zur Therapie der Neuropathia diabetica. Munch. Med. Wochenschr. 1959, 43, 1911–1912
Brookes, M.H.; Golding, B.T.; Howes, D.A.; Hudson, A.T. Proof that the absolute configuration of natural α-lipoic acid is R by the synthesis of its enantiomer [(S)-(–)-α-lipoic acid] from (S)-malic acid. J. Chem. Soc. Chem. Commun. 1983, 19, 1051–1053.
Ghibu, S.et al. L. Antioxidant properties of an endogenous thiol: Alpha-lipoic acid, useful in the prevention of cardiovascular diseases. J. Cardiovasc. Pharmacol. 2009, 54, 391–398. DOI: 10.1097/FJC.0b013e3181be7554
Brufani, M. Acido α-lipoico farmaco o integratore. Una panoramica sulla farmacocinetica, le formulazioni disponibili e le evidenze cliniche nelle complicanze del diabete. Prog. Nutr. 2014, 16, 62–74.
Szeląg, M.; Mikulski, D.; Molski, M. Quantum-chemical investigation of the structure and the antioxidant properties of α-lipoic acid and its metabolites. J. Mol. Modeling 2012, 18, 2907–2916. DOI: 10.1007/s00894-011-1306-y
Akiba, S.; Matsugo, S.; Packer, L.; Konishi, T. Assay of protein-bound lipoic acid in tissues by a new enzymatic method. Anal. Biochem. 1998, 258, 299–304. DOI: 10.1006/abio.1998.2615
Giacco, F.; Brownlee, M. Oxidative stress and diabetic complications. Circ. Res. 2010, 107, 1058–1070. [Google Scholar] [CrossRef] [PubMed]
Pitocco, D.; Tesauro, M.; Alessandro, R.; Ghirlanda, G.; Cardillo, C. Oxidative Stress in Diabetes: Implications for Vascular and Other Complications. Int. J. Mol. Sci. 2013, 14, 21525–21550. [Google Scholar] [CrossRef] [PubMed][Green Version]
Asmat, U.; Abad, K.; Ismail, K. Diabetes mellitus and oxidative stress-A concise review. Saudi Pharm. J. 2016, 24, 547–553. [Google Scholar] [CrossRef] [PubMed]
Eason, R.C.; Archer, H.E.; Akhtar, S.; Bailey, C.J. Lipoic acid increases glucose uptake by skeletal muscles of obesediabetic ob/ob mice. Diabetes Obes. Metab. 2002, 4, 29–35. DOI: 10.1046/j.1463-1326.2002.00171.x
Golbidi, S,. Badran, M,. Laher, I. Diabetes and alpha lipoic acid. Frontiers in pharmacology. 2011. DOI: 10.3389/fphar.2011.00069
Tibullo, D et al. Biochemical and clinical relevance of alpha lipoic acid: antioxidant and anti-inflammatory activity, molecular pathways and therapeutic potential. Inflammation Research. 2017. DOI: 10.1007/s00011-017-1079-6
Cromheeke, KM et al. Inducible nitric oxide synthase colocalizes with signs of lipid oxidation/peroxidation in human atherosclerotic plaques. Cardiovasc Res. 1999;43(3):744–54. DOI: 10.1007/s00011-017-1079-6
Wenk GL. Neuropathologic changes in alzheimer’s disease: potential targets for treatment. J Clin Psychiatry. 2006;67(Suppl 3):3–7 (quiz 23).
Abdul HM, Butterfield DA. Involvement of PI3K/PKG/ERK1/2 signaling pathways in cortical neurons to trigger protection by cotreatment of acetyl-L-carnitine and alpha-lipoic acid against
HNE-mediated oxidative stress and neurotoxicity: implications for alzheimer’s disease. Free Radic Biol Med. 2007;42(3): 371–84. DOI: 10.1016/j.freeradbiomed.2006.11.006
Al Abdan M. Alfa-lipoic acid controls tumor growth and modulates hepatic redox state in Ehrlich-ascites-carcinoma-bearing mice. Sci World J. 2012;2012:509838.
Feuerecker B, Pirsig S, Seidl C, Aichler M, Feuchtinger A, Bruchelt G, Senekowitsch-Schmidtke R. Lipoic acid inhibits cell proliferation of tumor cells in vitro and in vivo. Cancer Biol Ther. 2012;13(14):1425–35
Guais A, Baronzio G, Sanders E, Campion F, Mainini C, Fiorentini G, Montagnani F, Behzadi M, Schwartz L, Abolhassani M. Adding a combination of hydroxycitrate and lipoic acid (METABLOC) to chemotherapy improves effectiveness against tumor development: experimental results and case report. Invest New Drugs. 2012;30(1):200–11
Kim JI, Cho SR, Lee CM, Park ES, Kim KN, Kim HC, Lee HY. Induction of ER stress-mediated apoptosis by alpha-lipoic acid in A549 cell lines. Korean J Thorac Cardiovasc Surg. 2012;45(1):1–10.
Merz PA, Wisniewski HM, Somerville RA, Bobin SA, Masters L, Iqbal K. Ultrastructural morphology of amyloid fibrils from neuritic and amyloid plaques. Acta Neuropathol. 1983;60(1–2):113–24.
Michikoshi H, Nakamura T, Sakai K, Suzuki Y, Adachi E, Matsugo S, Matsumoto K. alpha-Lipoic acid-induced inhibition of proliferation and met phosphorylation in human non-small cell lung cancer cells. Cancer Lett. 2013;335(2):472–8.
Durand M, Mach N. Alpha lipoic acid and its antioxidant against cancer and diseases of central sensitization. Nutr Hosp. 2013;28(4):1031–8
Holmquist L, Stuchbury G, Berbaum K, Muscat S, Young S, Hager K, Engel J, Munch G. Lipoic acid as a novel treatment for alzheimer’s disease and related dementias. Pharmacol Ther. 2007;113(1):154–64.
Yang, L.; Wen, Y.; Lv, G.; Lin, Y.; Tang, J.; Lu, J.; Zhang, M.; Liu, W.; Sun, X. a-Lipoic acid inhibits human lung cancer cell proliferation through Grb2-mediated EGFR down regulation. Biochem. Biophys. Res. Commun. 2017, 494, 325–331
Salomone F, Barbagallo I, Puzzo L, Piazza C, Li Volti G. Efficacy of adipose tissue-mesenchymal stem cell transplantation in rats with acetaminophen liver injury. Stem Cell Res. 2013;11(3):1037–44.
San-Millán, I; Brooks, A. G. Reexamining cancer metabolism: lactate production for carcinogenesis could be the purpose and explanation of the Warburg Effect. Carcinogenesis. v 38, c 2. 2017. p 119–133. DOI: 10.1093/carcin/bgw127
Hermann, R.; Niebch, G.; Borbe, H.O.; Fieger-Büschges, H.; Ruus, P.; Nowak, H.; Riethmüller-Winzen, H.; Peukert, M.; Blume, H. Enantioselective pharmacokinetics and bioavailability of different racemic α-lipoic acid formulations in healthy volunteers. Eur. J. Pharmacol. Sci. 1996, 4, 167–174.
Ziegler D, Nowak H, Kempler P, Vargha P, Low PA. Treatment of symptomatic diabetic polyneuropathy with the antioxidant alpha-lipoic acid: a meta-analysis. Diabet Med. 2004 (2):114-21. DOI: 10.1111/j.1464-5491.2004.01109.x
Sen, C. K et al. Regulation of cellular thiols in human lymphocytes by alpha-lipoic acid: a flow cytometric analysis. Free Radic Biol Med. 1997;22(7):1241-57. DOI:10.1016/s0891-5849(96)00552-7
Heitzer, T et al. Beneficial effects of alpha-lipoic acid and ascorbic acid on endothelium-dependent, nitric oxide-mediated vasodilation in diabetic patients: relation to parameters of oxidative stress. Free Radic Biol Med. 2001. 31(1):53-61. DOI: 10.1016/s0891-5849(01)00551-2.
Ziegler, D et al. Treatment of symptomatic diabetic peripheral neuropathy with the antioxidant α-lipoic acid. A 3-week multicentre randomized controlled trial. Diabetologia. 1995. (38) 1425–1433.
Ziegler, D et al. Treatment of symptomatic diabetic polyneuropathy with the antioxidant α-lipoic acid. An 7-month multicenter randomized controlled trial. Diabetes Care. 1999 (22) 1296–1301.
Ametov, A et al. The sensory symptoms of diabetic polyneuropathy are improved with α-lipoic acid. Diabetes Care. 2003 (26) 770–776.
Nagamatsu, M et al. Lipoic acid improves nerve blood flow, reduces oxidative stress and improves distal nerve conduction in experimental diabetic neuropathy. Diabetes Care. 1995. (18)1160–1167. DOI: 10.2337/diacare.18.8.1160
Kozlov, A. V et al. Dihydrolipoic acid maintains ubiquinone in the antioxidant active form by two-electron reduction of ubiquinone and one electron reduction of ubisemiquinone. Arch Biochem Biophys. 1999, 363(1):148–154. DOI: 10.1006/abbi.1998.1064
Murase, K,. Hattori, A,. Kohno M, Hayashi, K. Stimulation of nerve growth factor synthesis/secretion in mouse astroglial cells by coenzymes. Biochem Mol Biol Int. 1993 Jul;30(4):615-21
Cremer DR, Rabeler R, Roberts A, Lynch B. Safety evaluation of alpha-lipoic acid (ALA). Regul Toxicol Pharmacol. 2006.46(1):29-41
Vigil, M,. Berkson, B. M,. Garcia, A. P. Adverse effects of high doses of intravenous alpha lipoic Acid on liver mitochondria. Glob Adv Health Med. 2014 Jan;3(1):25-7.
Nguyen H , Gupta V. Alpha-Lipoic Acid. StatPearls. StatPearls Publishing, Treasure Island (FL); 2020. PMID: 33231971
Carter, D. Osborne, V, Anderson, P,. A scientific reference for intravenous nutrient therapy: direct cellular nutrition. 2022


Comentários