A relação entre o relógio
biológico e a nutrição
Acesso rápido
O relógio biológico humano
Estímulo à melatonina
Variações do sono e consequências metabólicas
Qualidade do sono
Sono de longa e curta duração
Relação entre relógio biológico e apetite
Horário de ingestão alimentar
Regularidade e número de refeições
Número de refeições e sono
Aplicação clínica
Conteúdos relacionados
O equilíbrio no funcionamento do relógio biológico é importante para a manutenção da saúde de modo geral. As oscilações hormonais que acontecem durante o dia e durante a noite podem influenciar diretamente em questões como perda ou ganho de peso, apetite, qualidade do sono e sensibilidade à insulina.
O relógio biológico humano
Nos mamíferos existe um relógio biológico central, o núcleo supraquiasmático, que é regulado principalmente pela presença ou ausência de luz e que controla a estimulação da secreção de melatonina pela glândula pineal, sinalizando ao organismo qual é a função fisiológica que ele deve ter no momento.
Segundo a cronobiologia, o relógio biológico central também sincroniza os relógios periféricos, que se encontram em órgãos como o fígado, o rim, o coração, o pulmão, o tecido adiposo, o pâncreas, o intestino e o músculo. Ainda, o relógio central responde aos sinais de luz e escuridão, enquanto os periféricos reagem à ingestão de alimentos, ao sono, ao exercício físico e ao jejum.
A sincronização do relógio biológico pode ser influenciada positivamente ou negativamente por alguns fatores, como padrões alterados de ingestão alimentar, exposição prolongada à luz artificial e restrição de sono, além do trabalho em turno noturno.
As alterações trazidas pela vida moderna, como os estímulos noturnos, a abundância na oferta de alimentos e um maior sedentarismo, também afetam o funcionamento natural dos ritmos biológicos. De acordo com a literatura, essas variações podem aumentar a chance de doenças crônicas não transmissíveis, como diabetes tipo 2, arteriosclerose, obesidade, dislipidemia e esteatose.

Estímulo à melatonina
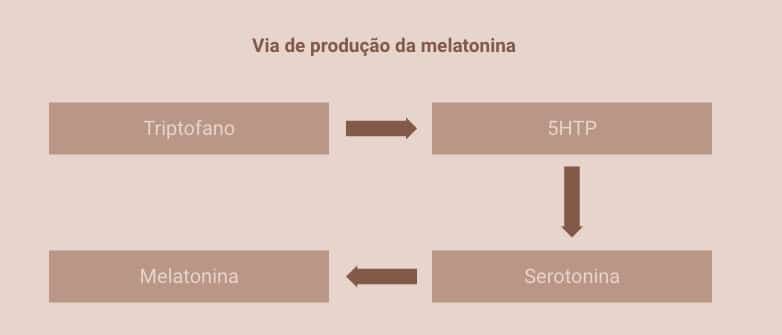
A melatonina é um dos principais marcadores do ritmo circadiano. Além dos efeitos no ritmo circadiano e no sono, a melatonina parece benéfica também na regulação do perfil lipídico, resistência à insulina, microbiota intestinal e inflamação. Dessa forma, pode estar relacionada à regulação do peso corporal, pois estimula a secreção e ação da insulina.
Os níveis de melatonina começam a aumentar no início da noite, atingindo os valores máximos entre as 2 e as 4 horas da manhã. A partir daí, decrescem e são mínimos durante o dia.
Variações do sono e
consequências metabólicas
Distúrbios de sono estão relacionados ao aumento dos níveis de cortisol à noite e à diminuição dos níveis de leptina e da tolerância à glicose. Também há associação com alterações nas concentrações da insulina e o desenvolvimento de diabetes tipo 2 e obesidade.

Qualidade do sono
Um estudo brasileiro realizado em Santa Catarina (Quadra et al., 2022) avaliou a influência do sono relacionado à crononutrição na hipertensão arterial sistêmica (HAS) e diabetes mellitus (DM). Os autores observaram que 36,1% dos participantes tinham longa duração do sono e 16,3% tinham curta duração. Com relação à qualidade, 48,2% referiu qualidade ruim do sono, sendo mais prevalente em mulheres (p = 0,041).
A qualidade ruim do sono associou-se positivamente com DM e HAS, onde indivíduos com pior qualidade do sono apresentaram prevalências 33% maior para DM (RP: 1,33; IC95%: 1,01-1,75) e 17% maior para HAS (RP: 1,17; IC95%: 1,02-1,34) quando comparados aos indivíduos com boa qualidade do sono, ajustado para fatores de confusão.
Os pesquisadores destacaram que cronorrupturas e desregulações do sono parecem estar associadas ao mau funcionamento dos sistemas, levando a alterações hormonais e prejuízos na função pancreática, disfunção de adipócitos, aumento de citocinas inflamatórias e diminuição da taxa metabólica em repouso. Além disso, também incentivam o aumento do consumo alimentar, o que favorece a diminuição da tolerância à glicose e a resistência à insulina, aumentando o risco de desenvolvimento de DM.
Também parece haver influência do ciclo vigília-sono no controle da pressão arterial. Normalmente, essa aumenta lentamente ao final do período de sono e rapidamente no início do período de vigília, e apresenta dois picos diurnos, reduzindo novamente ao se aproximar do período de sono. A síntese de melatonina, o sistema nervoso central e o sistema renina-angiotensina-aldosterona influenciam nos mecanismos regulatórios da pressão e, assim, cronodesregulações levariam ao aumento das catecolaminas, relacionadas à HAS.

Sono de longa e curta duração
A longa duração do sono também parece ser um fator negativo: uma revisão sistemática com metanálise identificou que o sono de longa duração (mais do que 9 horas) apresenta resultados adversos para a saúde, como mortalidade, incidência de DM, HAS, doenças cardiovasculares, acidente vascular cerebral e obesidade. Assim, tanto o sono curto (menor que 6 horas) quanto o sono longo são prejudiciais à saúde e estão associados à maior probabilidade de doenças crônicas.
Nesse sentido, uma grande pesquisa realizada com 11.842 indivíduos chineses explorou as interações entre a qualidade e duração do sono no desenvolvimento de DM2. O risco relativo para o desenvolvimento da doença foi maior nas pessoas com curta duração do sono (1,67 [1,34-2,16]) ou má qualidade do sono (1,91 [1,31-2,74]) ou longa duração do sono (1,45 [1,02-1,77]). Ainda, o DM2 ocorreu mais frequentemente com má qualidade do sono combinada com curta duração (OR: 6,21; IC95%: 2,78-11,81.)
Relação entre relógio biológico e apetite
Pesquisadores defendem que o relógio periférico do tecido adiposo controla oscilações circadianas de leptina, glicose, triglicerídeos, ácidos graxos livres e colesterol LDL no plasma. A leptina, especificamente, é um dos reguladores das sensações de fome e saciedade. Ela apresenta níveis elevados no plasma sanguíneo à noite, quando o apetite diminui, favorecendo a fase de jejum e descanso. Sua menor concentração ao longo do dia favorece a sensação de fome. Entretanto, a restrição do sono e seu impacto no relógio biológico podem afetar os níveis de leptina, contribuindo para o aumento do apetite.
Outro hormônio envolvido na estimulação do apetite é a grelina. Sua concentração no plasma também é maior durante as primeiras fases da noite de sono, decrescendo de manhã antes do acordar. Estudos in vitro mostraram que ela também pode alterar a “função relógio” dos núcleos supraquiasmáticos. Como sua concentração também varia com a alimentação, ela tem potencial para ser considerada como um hormônio sincronizador relacionado com alimentos.
Apesar de o organismo trabalhar para manter o balanço energético, a frequente alteração no relógio biológico pode afetar essa capacidade. Duas noites de interrupção de sono podem reduzir a tolerância à glicose e aumentar o apetite para alimentos hipercalóricos, sugerindo que o desalinhamento circadiano desencadeia um déficit energético que leva o organismo a ativar um processo obesogênico, como forma de compensação.
Horário de ingestão alimentar
Muitas vertentes recomendam que a ingestão alimentar seja feita principalmente no período diurno e em menor proporção no período da noite. Isso ocorre porque, durante a noite, na fase de jejum noturno, os genes ativos estão ligados ao crescimento e reparo, à glicogenólise e à lipólise. Já durante o dia, os genes ativos estão relacionados à glicogênese e lipogênese, devido à ação da insulina, com a finalidade de repor os estoques de energia, ou seja, o organismo está mais preparado para receber maior volume calórico:
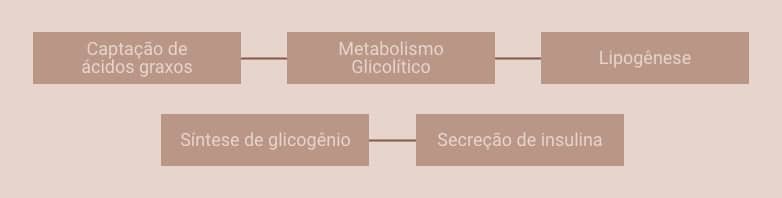
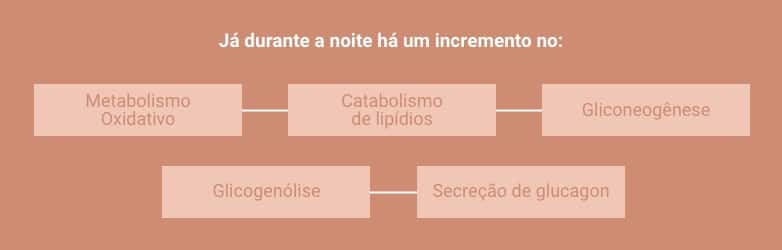
De acordo com uma revisão de literatura sobre o tema, o desalinhamento entre a ingestão de alimentos e os processos circadianos pode prejudicar a capacidade do organismo em manter seu equilíbrio energético. Evidências apontam que comer tarde da noite está associado à diminuição do gasto energético em repouso, diminuição da oxidação de carboidratos em jejum e da tolerância à glicose, afetando o ciclo circadiano. Além disso, um maior fracionamento de refeições durante o dia (6 ou mais) pode estar associado à melhor qualidade da dieta e menor IMC e uma maior ingestão noturna em relação à matinal está associada ao aumento do IMC.
Nesse sentido, a homeostase da glicose e dos lipídios, bem como a sensibilidade à insulina, o gasto energético e o apetite são controlados pelo sistema circadiano. Por isso, o alinhamento dos horários de ingestão alimentar é uma estratégia para melhorar a saúde metabólica. A tolerância à glicose, por exemplo, atinge seu pico máximo de secreção durante o ciclo do dia e o mínimo durante a noite. A insulina é produzida de acordo com um controle temporal, sendo liberada tanto em resposta aos padrões de alimentação-jejum, quanto pelo ritmo biológico. Os níveis máximos de cortisol são sincronizados com o início da fase ativa do dia em animais diurnos.
Regularidade e número de refeições
Alguns estudos defendem que um maior número de refeições pode ser protetor contra o sobrepeso ou obesidade, enquanto outros afirmam que é um fator que estimula o aumento do peso. Existem ainda os que concluem que não há associação entre o número diário de refeições e o peso corporal.
Evidências mais recentes, no entanto, sugerem que o mais importante é a regularidade das refeições e dos seus intervalos e não especificamente a sua frequência. Estudos mostram que um padrão irregular de refeições pode ter efeitos negativos na sensibilidade à insulina, nos lípidos plasmáticos e no balanço energético, constituindo um fator de risco cardiovascular. Por outro lado, um padrão regular previne flutuações nas concentrações de glicose e insulina no plasma, evitando a sensação de fome.
O estudo de Quadra e colaboradores (2022) também verificou a relação entre o comportamento alimentar, DM e HAS. Constatou-se que os indivíduos que realizavam quatro ou mais refeições ao dia apresentaram prevalência 16% menor de HAS (RP: 0,84; IC95%: 0,70-0,99), quando comparados àqueles que faziam menos de quatro refeições diárias. O maior número de refeições diárias está associado à melhor qualidade da dieta, com maior ingestão de vegetais e frutas, evidenciando um padrão alimentar protetor para doenças metabólicas.

Número de refeições e sono
Uma pesquisa realizada com 1.081 adultos brasileiros descreveu o consumo e comportamento alimentar e investigou as associações com a duração do sono. Menos da metade (47,6%) dos entrevistados apresentou duração adequada do sono (7-8h).
Observou-se que os indivíduos que dormiam por curtos períodos (6 horas ou menos) apresentaram comportamentos caracterizados por longo período de alimentação, alta frequência alimentar e um alto número de lanches com alto teor de energia e açúcar. Já os que dormiam por longos períodos (9 horas ou mais) apresentaram curto período de alimentação, baixa frequência alimentar e baixa probabilidade de consumo das três principais refeições (café da manhã, almoço e jantar). Aqueles com sono adequado tinham maior probabilidade de consumir as três principais refeições.
Para todos os indivíduos, a maior contribuição para a ingestão total de energia ocorreu à tarde (43-46%) e à noite (30-32%). Esses dados reforçam a importância de um aconselhamento nutricional que leva em consideração o momento do consumo alimentar como forma de prevenir o desalinhamento circadiano e dos distúrbios metabólicos relacionados ao aumento do risco de obesidade e de outras condições metabólicas.
Aplicação clínica
O relógio biológico parece um recurso potencial na prática clínica para prevenir e tratar indivíduos em risco de doenças metabólicas, além de promover o bem-estar e a longevidade. O foco dessa abordagem baseia-se na estimulação dos sincronizadores circadianos, com estratégias que envolvem alimentação, jejum, sono, luz artificial e atividade física.
Dessa forma, os ritmos biológicos diários e a saúde metabólica podem ser melhorados a partir dos horários adequados de alimentação, da ocasião de comer (pular refeições, quantidade e tipo de macronutrientes) e da duração/restrição do sono, por exemplo.
IMPORTANTE
Este material é de apoio técnico para prescritores e é proibida a sua divulgação para consumidores, nos termos do item 5.14 da RDC 67/2007.
Conteúdos relacionados
POTTER, Gregory D. M. et al. Circadian Rhythm and Sleep Disruption: causes, metabolic consequences, and countermeasures. Endocrine Reviews, v. 37, n. 6, p. 584-608, 2016.
QUADRA, Micaela Rabelo et al. Influência do sono e da crononutrição na hipertensão e diabetes: um estudo de base populacional. Cadernos de Saúde Pública, v. 38, n. 7, 2022.
COSTA, Cynthia Giovanni A. D. C.; SOARES, Poliana Oliveira; ALMEIDA, Simone Gonçalves de. O Papel da crononutrição nas desordens do metabolismo: uma revisão de literatura. Research, Society And Development, v. 12, n. 6, 2023.
MASON, Ivy C. et al. Impact of circadian disruption on glucose metabolism: implications for type 2 diabetes. Diabetologia, v. 63, n. 3, p. 462-472, 2020.
JIKE, Maki et al. Long sleep duration and health outcomes: a systematic review, meta-analysis and meta-regression. Sleep Medicine Reviews, v. 39, p. 25-36, 2018.
LOU, Peian et al. Effects of sleep duration and sleep quality on prevalence of type 2 diabetes mellitus: a 5-year follow-up study in china. Diabetes Research And Clinical Practice, v. 109, n. 1, p. 178-184, 2015.
CASTRO, Michelle Alessandra de et al. Eating behaviours and dietary intake associations with self-reported sleep duration of free-living Brazilian adults. Appetite, v. 137, p. 207-217, 2019.





BOM DIA.
Almejo APROFUNDAR CONHECIMENTO SOBRE OS TEMAS EXPOSTOS, ASSIM DE IMEDIATO PARA COMEÇAR ME INCREVER NO CURSO DE 20HS E DIVULGAR.
Olá Dr Salomão, já encaminhei sua solicitação para o nosso setor responsável verificar e entrar em contato com você. Um grande abraço, Essentia Group
Boa leitura, colocado de uma forma simples e que pode trouxe muita bagagem.
Obrigada!
Olá Drª Sônia, agradecemos imensamente seu feedback ♥ Um grande abraço, Essentia Group
Muito bom o texto, parabéns
Olá Dr Matheus, agradecemos imensamente seu feedback ♥ Um grande abraço, Essentia Group